题目内容
8.下列说法正确的是( )| A. | 甲烷的燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知中和热为△H=-57.3kJ•mol-1,则稀醋酸和稀NaOH溶液反应的热化学方程式为:CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3 kJ•mol-1 |
分析 A.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,水的状态应该为液态;
B.固体硫转化为气态硫的过程是吸热的过程;
C.物质具有能量越高,物质的稳定性越差;
D.醋酸为弱酸,电离过程中需要吸热,则醋酸与氢氧化钠溶液反应放出的热量减少.
解答 解:A.1mol可燃物完全燃烧生成稳定的氧化物所放出的热量为燃烧热,水的状态应该为液态,正确的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1,故A错误;
B.固体硫转化为气态硫的过程是吸热的过程,所以等量的气态硫燃烧放热多,而焓变为负值,则△H1<△H2,故B正确;
C.已知C(石墨,s)═C(金刚石,s)△H>0,该反应为吸热反应,说明石墨具有的能量小于金刚石,则金刚石不如石墨稳定,故C错误;
D.已知中和热为△H=-57.3kJ•mol-1,由于醋酸电离吸热,则稀醋酸和稀NaOH溶液反应放热的热量减少,则该反应的热化学方程式为:CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H>-57.3 kJ•mol-1,故D错误;
故选B.
点评 本题考查了热化学方程式的书写、反应热与焓变的应用,题目难度中等,明确燃烧热、中和热的概念为解答关键,注意掌握热化学方程式的书写原则.

练习册系列答案
相关题目
18.下列物质不含有共价键的是( )
| A. | NaCl | B. | CO2 | C. | NaOH | D. | O3 |
19.下列说法正确的是( )
| A. | 乙烯的结构简式为CH2CH2 | B. | 烃类分子中可能含有氧元素 | ||
| C. | 化学用语:乙酸乙脂笨 | D. | 烷烃的通式为CnH2n+2 |
13.在 100mL 0.10mol•L-1的 AgNO3(aq) 中,加入 100mL 溶有 2.08g BaCl2 的溶液,再加入 100mL 溶有 2.50g CuSO4•5H2O 的溶液,充分反应.下列说法中正确的是( )
| A. | 最终得到白色沉淀和无色溶液 | |
| B. | 最终得到的白色沉淀是等物质的量的两种化合物的混合物 | |
| C. | 混合过程中,逸出无色气体 | |
| D. | 在最终得到的溶液中,c(Cu2+)=0.01 mol•L-1 |
20.下列各组物质中,X是主体物质,Y是少量杂质,Z是要除去杂质而加入的试剂,其中正确的组别是( )
| X | Y | Z | |
| A | FeCl2溶液 | FeCl3 | KSCN溶液 |
| B | Fe粉 | A1粉 | HC1溶液 |
| C | Fe2(SO4)3溶液 | FeSO4 | C12 |
| D | FeCl2溶液 | CuCl2 | Fe粉 |
| A. | A | B. | B | C. | C | D. | D |
17.用NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 11.2LCO和N2混合气体中含有的分子数是0.5NA | |
| B. | 在氯气参与的反应中,22.4L(标况)氯气完全反应得到的电子数一定为0.2NA | |
| C. | 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 | |
| D. | l L l mol•L-1的NaClO溶液中含有ClO-的数目小于NA |
18.2015年巴黎气候变化大会规定:本世纪实现温室气体净零排放.下列物质燃烧时能实现二氧化碳零排放的是( )
| A. | 天然气 | B. | 氢气 | C. | 水煤气 | D. | 煤炭 |


 .
.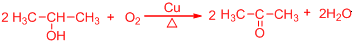 .
.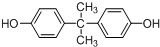 所示,下列说法正确的是ab.
所示,下列说法正确的是ab. .
.
 (其中两种)
(其中两种)