题目内容
将0.2mol?L-1MOH溶液和0.1mol?L-1HCl的溶液等体积混合后,溶液呈酸性,下列关系式中不正确的是( )
| A、c(MOH)>c(M+) |
| B、c(M+)+c(H+)=c(Cl-)+c(OH-) |
| C、c(MOH)+c(M+)=0.2mol?L-1 |
| D、c(M+)<c(Cl-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:将0.2mol?L-1MOH溶液和0.1mol?L-1HCl的溶液等体积混合后,得浓度均为0.05mol/L的MCl和MOH的混合溶液,根据溶液显酸性可知MCl的水解大于MOH的电离,根据两者在溶液中的行为来分析.
解答:
解:将0.2mol?L-1MOH溶液和0.1mol?L-1HCl的溶液等体积混合后,得浓度均为0.05mol/L的MCl和MOH的混合溶液,根据溶液显酸性可知MCl的水解大于MOH的电离,根据两者在溶液中的行为可知:M++H2O?MOH+H+(主),MOH?M++OH- (次),
A、由于混合溶液中本来MCl和MOH的浓度均为0.05mol/L,但由于MCl的水解大于MOH的电离,导致溶液中c(MOH)>c(M+),故A正确;
B、混合溶液中的离子有:M+、H+、OH- 和Cl-,根据电荷守恒可知:c(M+)+c(H+)=c(Cl-)+c(OH-),故B正确;
C、混合溶液中MCl和MOH的浓度均为0.05mol/L,根据物料守恒可知:c(MOH)+c(M+)=0.1mol?L-1,故C错误;
D、混合溶液中MCl和MOH的浓度均为0.05mol/L,故溶液中C(Cl-)=0.05mol/L,而MCl的水解大于MOH的电离,导致比c(M+)比0.05mol/L小,即小于氯离子浓度,故D正确.
故选C.
A、由于混合溶液中本来MCl和MOH的浓度均为0.05mol/L,但由于MCl的水解大于MOH的电离,导致溶液中c(MOH)>c(M+),故A正确;
B、混合溶液中的离子有:M+、H+、OH- 和Cl-,根据电荷守恒可知:c(M+)+c(H+)=c(Cl-)+c(OH-),故B正确;
C、混合溶液中MCl和MOH的浓度均为0.05mol/L,根据物料守恒可知:c(MOH)+c(M+)=0.1mol?L-1,故C错误;
D、混合溶液中MCl和MOH的浓度均为0.05mol/L,故溶液中C(Cl-)=0.05mol/L,而MCl的水解大于MOH的电离,导致比c(M+)比0.05mol/L小,即小于氯离子浓度,故D正确.
故选C.
点评:本题考查了在酸碱混合之后溶液中离子浓度的大小比较,应注意混合后溶液体积的变化对溶质浓度的影响,难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
 2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )
2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )| A、0.01mol?L-1的醋酸溶液的pH=2 |
| B、向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka会增大 |
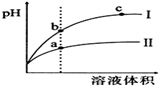
| C、等pH的盐酸与醋酸稀释后pH的变化如下图所示,则曲线I表示的是盐酸 |
| D、上图中,a、b、c三点表示的溶液的导电性强弱关系为b>a>c |
有关纤维素的说法,错误的是( )
| A、纤维素是一种天然高分子化合物 |
| B、纤维素是一种多糖,能够水解生成葡萄糖 |
| C、人体内含有能够促使纤维素水解的酶,纤维素在人体内能够被消化吸收 |
| D、纤维素是白色、没有气味和味道的纤维状结构的物质 |
2011年6月,云南省曲靖市发生了铬渣污染事件.在金属零件上镀铬后,既可以增加硬度,也可以有装饰的效果.如果在CrCl3溶液中,在铁制零件上镀铬,镀铬的阳极不用金属铬,而采用不溶性阳极.以下说法中正确的是( )
| A、铁制零件应该连接电源的负极 |
| B、阳极发生的电极反应为:Cr3++3e-=Cr |
| C、为了增强溶液的导电性,可以向溶液中加入一些溶于水的强电解质,提高溶液的pH |
| D、当通过1.5mol e-时,铁制零件上可沉积78g铬镀层 |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.25molCu(OH)2固体后恰好恢复到电解前的浓度和pH.则电解过程中共转移电子的物质的量为( )
| A、0.25 mol |
| B、0.5 mol |
| C、0.75 mol |
| D、1.0mol |
生活中涉及的许多问题与化学有关,下列说法不正确的是( )
| A、“白色污染”是指塑料包装袋等塑料垃圾 |
| B、碘盐中的碘不是碘单质 |
| C、“绿色食品”是指绿色的食品 |
| D、工业酒精中因含较多甲醇,故严禁饮用 |