题目内容
下列说法正确的是( )
| A、二氧化碳溶于水可以导电,所以二氧化碳是电解质 |
| B、液态氯化氢不能导电,所以氯化氢是非电解质 |
| C、Na2O2与水反应能生成碱,所以它是碱性氧化物 |
| D、FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
考点:电解质与非电解质,酸、碱、盐、氧化物的概念及其相互联系,化学试剂的存放
专题:电离平衡与溶液的pH专题,元素及其化合物
分析:A.电解质为:在水溶液中或熔融状态下能够导电的化合物,电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;
非电解质为:在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子;
B.根据电解质、非电解质概念分析;
C.过氧化钠属于过氧化物;
D.根据亚铁盐容易被氧化,则保存时应注意加入还原性铁来防止亚铁离子被氧化.
非电解质为:在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子;
B.根据电解质、非电解质概念分析;
C.过氧化钠属于过氧化物;
D.根据亚铁盐容易被氧化,则保存时应注意加入还原性铁来防止亚铁离子被氧化.
解答:
解:A、CO2在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子,溶液能够导电,但自由移动的离子不是CO2自身电离,故CO2是非电解质,故A错误;
B、氯化氢在溶液中能够电离出氢离子和氯离子,属于电解质,故B错误;
C、Na2O2能与酸反应生成盐、水和氧气,过氧化钠属于过氧化物,故C错误;
D、FeSO4中Fe为+2价,所以极易被氧化为+3价,加入铁粉后,会与+3价的铁反应使之成为亚铁离子后,融入到FeSO4溶液中,这样便有效地减少FeSO4的损失,故D正确;故选D.
B、氯化氢在溶液中能够电离出氢离子和氯离子,属于电解质,故B错误;
C、Na2O2能与酸反应生成盐、水和氧气,过氧化钠属于过氧化物,故C错误;
D、FeSO4中Fe为+2价,所以极易被氧化为+3价,加入铁粉后,会与+3价的铁反应使之成为亚铁离子后,融入到FeSO4溶液中,这样便有效地减少FeSO4的损失,故D正确;故选D.
点评:本题考查电解质与非电解质判断,氧化物的概念和化学试剂的保存,题目难度不大,注意解答该类概念性题目,关键是明确概念,抓住概念中的关键词,注意单质和混合物既不是电解质,也不是非电解质.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
下列关于糖的叙述不 正确的是( )
| A、多糖一般不溶于水,没有甜味 |
| B、最重要的多糖是淀粉和纤维素,二者通式是(C6H10O5)n |
| C、符合通式(C6H10O5)n的多糖互为同分异构体 |
| D、淀粉和纤维素在一定条件下水解,最终的产物都得到葡萄糖 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L SO3中所含有分子数为NA |
| B、常温下,28 g 乙烯和丙烯的混合物中所含化学键一定为6NA |
| C、在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定为4NA |
| D、1 L 1mol/L NH4NO3溶液中氮原子数目小于2NA |
某元素在化学反应中由化合态变为游离态,则该元素( )
| A、一定被氧化了 |
| B、一定被还原了 |
| C、既可能被氧化也可能被还原 |
| D、既不可能被氧化,也不可能被还原 |
下列有关试剂的保存方法错误的是( )
| A、少量的钠保存在煤油中 |
| B、新制的氯水保存在棕色试剂瓶中 |
| C、漂白粉要密闭保存 |
| D、浓盐酸保存在敞口试剂瓶中即可 |
下列化学用语表达不正确的是( )
A、次氯酸的电子式: | ||||
B、质子数为6、质量数为14的原子:
| ||||
| C、CS2的结构式:S-C-S | ||||
D、氯的原子结构示意图: |
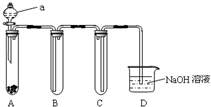 如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置. (提示:在酸性条件下MnO4-被还原为Mn2+)
如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置. (提示:在酸性条件下MnO4-被还原为Mn2+) 已知水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”可用如图表达:
已知水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”可用如图表达: