题目内容
甲烷-氧气燃料电池,该电池用金属铂片插入KOH溶液中作电极,在两极上分别通甲烷和氧气.该电池工作时:
负极反应式为: .
正极反应式为: .
电池总反应式为: .
负极反应式为:
正极反应式为:
电池总反应式为:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:甲烷燃料电池中,负极上投放燃料甲烷,发生失电子发生氧化反应,正极上投放氧气,发生得电子的还原反应,总反应是燃料和氧气反应的化学方程式,即为正极反应和负极反应的和,注意电解质环境决定方程式的书写.
解答:
解:在碱性溶液中,负极上投放燃料甲烷,发生失电子发生氧化反应:CH4-8e-+10OH-═CO32-+7H2O,正极上投放氧气,发生得电子的还原反应:2O2+4H2O+8e-═8OH-,燃料电池的总反应式为CH4+2O2+2OH-=CO32-+3H2O,
故答案为:CH4-8e-+10OH-═CO32-+7H2O;2O2+4H2O+8e-═8OH-;CH4+2O2+2OH-=CO32-+3H2O.
故答案为:CH4-8e-+10OH-═CO32-+7H2O;2O2+4H2O+8e-═8OH-;CH4+2O2+2OH-=CO32-+3H2O.
点评:本题考查了化学电源新型电池,根据得失电子确定正负极上通入的气体,难点是电极反应式的书写,注意碱性条件下甲烷失电子不能生成氢离子,要生成碳酸根离子,为易错点.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
常温下0.1mol?L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A、加入适量的氢氧化钠固体 |
| B、将溶液稀释到原体积的10倍 |
| C、加入等体积0.2mol?L-1氨水 |
| D、降低溶液的温度 |
下列实验能达到实验目的且操作规范的是( )
A、 制取氢氧化铜 |
B、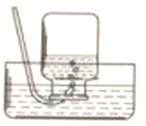 收集氧气 |
C、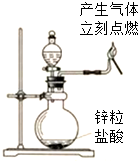 制取氢气并检验其可燃性 |
D、 点燃酒精灯 |
下列叙述正确的是( )
| A、金属元素的原子只有还原性,离子只有氧化性 |
| B、用乙烷(CH3CH3)或乙烯(CH2=CH2)制一氯乙烷(CH3CH2Cl)的反应类型相同 |
| C、煤油是通过煤干馏获得,可用作燃料和保存少量金属钠 |
D、 和CH3-CH=CH2互称为同分异构体 和CH3-CH=CH2互称为同分异构体 |


 如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化.每个小黑点代表一种氢化物,其中a点代表的是
如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化.每个小黑点代表一种氢化物,其中a点代表的是