题目内容
1.设阿伏加德罗常数的数值为NA,下列说法正确的是( )| A. | 0.1molNa2O2与水反应转移电子数为0.1 NA | |
| B. | 标准状况下,11.2L HF含有的分子数为0.5 NA | |
| C. | 1mol S在足量O2中燃烧,转移的电子数为6 NA | |
| D. | 7.8g Na2O2固体中所含阴离子数为2 NA |
分析 A.过氧化钠中氧元素的化合价为-1价,1mol Na2O2与水完全反应生成0.5mol氧气,转移了1mol电子;
B.标况下,HF不是气体;
C.硫与氧气反应生成二氧化硫,生成1mol二氧化硫转移4mol电子;
D.过氧化钠阴离子为过氧根离子.
解答 解:A.7.8g Na2O2固体物质的量为$\frac{7.8g}{78g/mol}$=0.1mol,转移了0.1mol电子,转移电子数为0.1 NA,故A正确;
B.标况下,HF不是气体,不能使用气体摩尔体积,故B错误;
C.1mol S在足量O2中燃烧生成1mol二氧化硫,转移的电子数为4 NA,故C错误;
D.7.8g Na2O2固体物质的量为$\frac{7.8g}{78g/mol}$=0.1mol,中所含过氧根离子数为0.1NA,故D错误;
故选:A.
点评 本题考查阿伏加德罗常数的有关计算和判断,明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得.工艺流程如图:
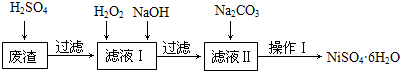
已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如表所示.
注:NiCO3是一种不溶于水易溶于强酸的沉淀.
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有AC.
A.升高反应温度B.增大压强C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示);加入NaOH调节pH的范围是5.6≤pH<8.4,为了除去溶液中的Fe3+、Cr3+离子.
(3)滤液Ⅱ的主要成分是Na2SO4、NiSO4.
(4)检验Ni2+已完全沉淀的实验方法是静置后向上层清液中再加入Na2CO3溶液后没有沉淀生成.
(5)操作Ⅰ的实验步骤依次为:
①过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性;
②向沉淀中加稀的H2SO4溶液,直至恰好完全溶解;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干.

已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如表所示.
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有AC.
A.升高反应温度B.增大压强C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示);加入NaOH调节pH的范围是5.6≤pH<8.4,为了除去溶液中的Fe3+、Cr3+离子.
(3)滤液Ⅱ的主要成分是Na2SO4、NiSO4.
(4)检验Ni2+已完全沉淀的实验方法是静置后向上层清液中再加入Na2CO3溶液后没有沉淀生成.
(5)操作Ⅰ的实验步骤依次为:
①过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性;
②向沉淀中加稀的H2SO4溶液,直至恰好完全溶解;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干.
6.判断下列有关化学基本概念的依据正确的是( )
| A. | 氧化还原反应:元素化合价是否变化 | |
| B. | 共价化合物:是否含有共价键 | |
| C. | 强弱电解质:溶液的导电能力大小 | |
| D. | 氧化物:含氧化合物 |
13.常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
下列判断正确的是( )
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.2 | 0.2 | pH=9 |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
| A. | c1=0.2 | |
| B. | 丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-) | |
| C. | a>9 | |
| D. | 在乙组混合液中由水电离出的c(OH-)=10-5mol•L-1 |
10.下列说法正确的是( )
| A. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 | |
| B. | 为增强氯水的漂白性,可以向其中加入碳酸钙 | |
| C. | NaH与重水反应的方程式:NaH+D2O═NaOH+D2↑ | |
| D. | 均含有NA个电子的H2O和CH4具有相同的体积 |
11.某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液a L与pH=1的H2SO4溶液b L混合(设混合溶液体积为两者之和,固体体积忽略不计).下列说法不正确的是( )
| A. | 若所得混合溶液为中性,则a:b=1:1 | |
| B. | 若所得混合溶液为中性,则生成沉淀的物质的量为0.05b mol | |
| C. | 若a:b=9:2,则所得溶液pH等于2 | |
| D. | 若a:b=9:2,则该混合溶液最多能溶解铁粉0.28(a+b)g |
 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.