题目内容
2.由二氧化硅制高纯硅的流程如下,下列判断中不正确的是( )
| A. | ①②③均属于氧化还原反应 | B. | H2和HCl均可循环利用 | ||
| C. | SiO2是一种坚硬难熔的固体 | D. | 硅可用于制作光导纤维 |
分析 A.有化合价变化的反应为氧化还原反应;
B.依据工艺流程判断;
C.二氧化硅为原子晶体,硬度较大;
D.光导纤维主要成分是二氧化硅.
解答 解:A.SiO2→Si,Si→SiHCl3,SiHCl3→Si,都存在化合价变化,都是氧化还原反应,故A正确;
B.依据工艺流程可知,氢气、氯化氢既参与反应,最终又生成,所以均可循环利用,故B正确;
C.二氧化硅为原子晶体,硬度较大,故C正确;
D.光导纤维主要成分是二氧化硅,故D错误;
故选:D.
点评 本题考查了硅及其化合物之间的转化,熟悉相关物质的性质是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4L CHCl3含氯原子数为3NA | |
| B. | 100mL 1 mol•L-1醋酸溶液中的氢原子数为0.4NA | |
| C. | 常温常压下,11.2g乙烯中共用电子对数为2.4NA | |
| D. | 6.4 g CaC2晶体中所含的离子总数为0.3NA |
13.下列开发利用自然资源制取化学品,其途径较合理的是( )
| A. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{高温}{→}$MgO$\stackrel{电解}{→}$Mg | |
| B. | 石油$\stackrel{裂解}{→}$$\stackrel{分馏}{→}$苯、甲苯、二甲苯、酚等 | |
| C. | 铝土矿$\stackrel{NaOH}{→}$$\stackrel{过滤}{→}$$\stackrel{盐酸}{→}$$\stackrel{过滤}{→}$Al(OH)3$\stackrel{灼烧}{→}$Al2O3$\stackrel{电解}{→}$Al | |
| D. | 海洋生物$\stackrel{灼烧}{→}$$\stackrel{浸取}{→}$$\stackrel{Cl_{2}}{→}$$\stackrel{萃取}{→}$$\stackrel{分离提纯}{→}$I2 |
10.下列排列顺序不正确的是( )
| A. | 原子半径:钠>硫>氯 | |
| B. | 最高价氧化物对应的水化物的酸性:HClO4>H2SO4>H3PO4 | |
| C. | 热稳定性:碘化氢>溴化氢>氯化氢 | |
| D. | 最高正化合价:氯>硫>磷 |
17.甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如下表,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素.下列判断正确的是( )
| 甲 | |||
| 丁 |
| A. | 原子半径:丙>丁 | |
| B. | 甲与丁的核外电子数相差10 | |
| C. | 氢氧化物碱性:丙>乙 | |
| D. | 甲、乙的最高价氧化物均是共价化合物 |
7.化学与人类日常生活、生产密切相关.下列说法正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| C. | 侯氏制碱法的最终产品是小苏打 | |
| D. | 明矾可用于水的杀菌、消毒 |
14.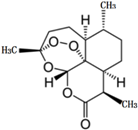 2015年10月,屠呦呦因青蒿素和双氢青蒿素的贡献,荣获2015年诺贝尔生理学或医学奖,成为第一位获得诺贝尔科学奖项的中国本土科学家.青蒿素的化学结构如图所示,下列说法不正确的是( )
2015年10月,屠呦呦因青蒿素和双氢青蒿素的贡献,荣获2015年诺贝尔生理学或医学奖,成为第一位获得诺贝尔科学奖项的中国本土科学家.青蒿素的化学结构如图所示,下列说法不正确的是( )
 2015年10月,屠呦呦因青蒿素和双氢青蒿素的贡献,荣获2015年诺贝尔生理学或医学奖,成为第一位获得诺贝尔科学奖项的中国本土科学家.青蒿素的化学结构如图所示,下列说法不正确的是( )
2015年10月,屠呦呦因青蒿素和双氢青蒿素的贡献,荣获2015年诺贝尔生理学或医学奖,成为第一位获得诺贝尔科学奖项的中国本土科学家.青蒿素的化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素的分子式为C15H21O5 | |
| B. | 由青蒿素分子中所含官能团推测,该物质难溶于水 | |
| C. | 在碱性条件下,青蒿素易发生水解反应 | |
| D. | 青蒿素因具有特殊的过氧基团,易受热和还原性物质的影响而分解 |
11.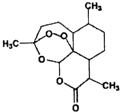 屠呦呦等科学家用乙醚从青蒿中提取出青蒿素,其结构如图所示,已知结构中含有与H2O2相似的过氧键.下列说法正确的是( )
屠呦呦等科学家用乙醚从青蒿中提取出青蒿素,其结构如图所示,已知结构中含有与H2O2相似的过氧键.下列说法正确的是( )
 屠呦呦等科学家用乙醚从青蒿中提取出青蒿素,其结构如图所示,已知结构中含有与H2O2相似的过氧键.下列说法正确的是( )
屠呦呦等科学家用乙醚从青蒿中提取出青蒿素,其结构如图所示,已知结构中含有与H2O2相似的过氧键.下列说法正确的是( )| A. | 青蒿素的结构中含有过氧键受热容易分解 | |
| B. | 乙醚的结构简式为:CH3OCH3 | |
| C. | 青蒿素溶于热水,所以应加热加快溶解 | |
| D. | 乙醚易溶于水,不能用分液的方法分离 |