题目内容
某课题组以苯为主要原料,采用以下路线合成利胆药-柳胺酚.
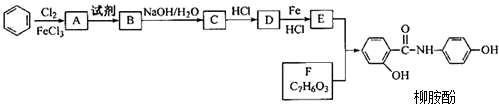
已知: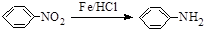 .请回答下列问题:
.请回答下列问题:
(1)对于柳胺酚,下列说法正确的是 .
A.1mol柳胺酚最多可以和2molNaOH反应 B.不发生硝化反应
C.可发生水解反应 D.可与溴发生取代反应
(2)写出A→B反应所需的试剂 .
(3)写出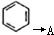 的化学方程式 .
的化学方程式 .
(4)写出化合物F的结构简式 .
(5)写出同时符合下列条件的F的同分异构体,其结构简式为 (写出3种).
①属酚类化合物,且苯环上有三种不同化学环境的氢原子; ②能发生银镜反应.

已知:
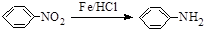 .请回答下列问题:
.请回答下列问题:(1)对于柳胺酚,下列说法正确的是
A.1mol柳胺酚最多可以和2molNaOH反应 B.不发生硝化反应
C.可发生水解反应 D.可与溴发生取代反应
(2)写出A→B反应所需的试剂
(3)写出
 的化学方程式
的化学方程式(4)写出化合物F的结构简式
(5)写出同时符合下列条件的F的同分异构体,其结构简式为
①属酚类化合物,且苯环上有三种不同化学环境的氢原子; ②能发生银镜反应.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:E与F合成柳胺酚,由柳胺酚分子结构与F的分子式,逆推可知F为 ,E为
,E为 ,D还原得到E,结合信息②可知,D为
,D还原得到E,结合信息②可知,D为 ,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为
,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为 ,A为
,A为 ,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为
,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为 ,据此解答.
,据此解答.
 ,E为
,E为 ,D还原得到E,结合信息②可知,D为
,D还原得到E,结合信息②可知,D为 ,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为
,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为 ,A为
,A为 ,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为
,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为 ,据此解答.
,据此解答.解答:
解:E与F合成柳胺酚,由柳胺酚分子结构与F的分子式,逆推可知F为 ,E为
,E为 ,D还原得到E,结合信息②可知,D为
,D还原得到E,结合信息②可知,D为 ,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为
,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为 ,A为
,A为 ,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为
,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为 ,
,
(1)柳胺酚分子中含酚羟基,具有酸性,含有酰胺键(类似于肽键),可以发生水解反应.
A.酚羟基及水解得到羧基均能与氢氧化钠反应,故1 mol柳胺酚最多可以 和3 mol NaOH反应.故A错误;
B.苯环上可以发生硝化反应,故B错误;
C.含有酰胺键(类似于肽键),可以发生水解反应,故C正确;
D.苯环上酚羟基邻、对位的氢可以发生溴代反应,故D正确,
故答案为:CD;
(2)A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,故反应所需的试剂为:浓硝酸和浓硫酸,
故答案为:浓硝酸和浓硫酸;
(3) 的化学方程式为
的化学方程式为 ,
,
故答案为: ;
;
(4)由上述分析可知,化合物F的结构简式为: ,故答案为:
,故答案为: ;
;
(5)F( )的同分异构体同时符合下列条件:属酚类化合物,且苯环上有三种不同化学环境的氢原子;能发生银镜反应,含有醛基或甲酸形成的酯基,符合条件的2种同分异构体为:
)的同分异构体同时符合下列条件:属酚类化合物,且苯环上有三种不同化学环境的氢原子;能发生银镜反应,含有醛基或甲酸形成的酯基,符合条件的2种同分异构体为: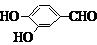 、
、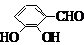 、
、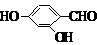 、
、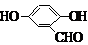 等,
等,
故答案为: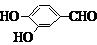 、
、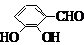 、
、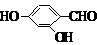 、
、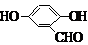 (其中三种).
(其中三种).
 ,E为
,E为 ,D还原得到E,结合信息②可知,D为
,D还原得到E,结合信息②可知,D为 ,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为
,由转化关系可知B中含有硝基,苯与氯气发生取代反应生成A,A与试剂X反应得到B,则B中含有氯原子、硝基,且处于对位,故B为 ,A为
,A为 ,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为
,A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,B发生水解反应生成C,C与HCl反应生成D,故C为 ,
,(1)柳胺酚分子中含酚羟基,具有酸性,含有酰胺键(类似于肽键),可以发生水解反应.
A.酚羟基及水解得到羧基均能与氢氧化钠反应,故1 mol柳胺酚最多可以 和3 mol NaOH反应.故A错误;
B.苯环上可以发生硝化反应,故B错误;
C.含有酰胺键(类似于肽键),可以发生水解反应,故C正确;
D.苯环上酚羟基邻、对位的氢可以发生溴代反应,故D正确,
故答案为:CD;
(2)A→B引入硝基,必有硝酸参与反应,还需浓硫酸做催化剂,故反应所需的试剂为:浓硝酸和浓硫酸,
故答案为:浓硝酸和浓硫酸;
(3)
 的化学方程式为
的化学方程式为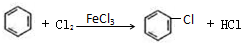 ,
,故答案为:
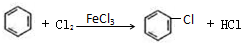 ;
;(4)由上述分析可知,化合物F的结构简式为:
 ,故答案为:
,故答案为: ;
;(5)F(
 )的同分异构体同时符合下列条件:属酚类化合物,且苯环上有三种不同化学环境的氢原子;能发生银镜反应,含有醛基或甲酸形成的酯基,符合条件的2种同分异构体为:
)的同分异构体同时符合下列条件:属酚类化合物,且苯环上有三种不同化学环境的氢原子;能发生银镜反应,含有醛基或甲酸形成的酯基,符合条件的2种同分异构体为: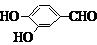 、
、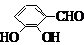 、
、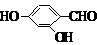 、
、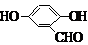 等,
等,故答案为:
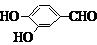 、
、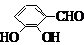 、
、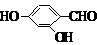 、
、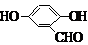 (其中三种).
(其中三种).
点评:本题考查了有机物的推断及合成,从柳胺酚的结构着手,采用逆推的方法推断各物质,明确反应时有机物的断键方式是解本题关键,难度中等.

练习册系列答案
相关题目
向体积为VL的NaALO2溶液中,开始通入amolHCl气体,则有bmol沉淀析出,继续通入cmolHCl气体后,产生的沉淀又恰好溶解,则原NaAlO2溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在VL硫酸铝溶液中,含有Wg Al3+离子,这种溶液中SO42-的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
将质量为W1克的钠、铝共融物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L.向溶液中逐滴加入浓度为a mol/L的HCl溶液,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2L.将溶液蒸干灼烧得固体W2克.n(Na)、n(Al)分别代表钠、铝的物质的量,下列关系式中不正确的是( )
| A、35.5aV2=W2-W1 |
| B、n(Al)<W1/50 |
| C、n(Na)+3n(Al)=2V1/22.4 |
| D、aV2=n(Na)+3n(Al) |
将a mol?L-1的Na2CO3溶液与b mol?L-1的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断不正确的是( )
| A、c(Na+)+c(H+)>c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b |
| D、若a=b,则溶液中c(HCO3-)>c(CO32-) |
下列装置或操作能达到实验目的是( )
A、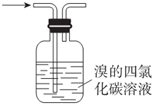 除去甲烷中乙烯 |
B、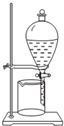 从碘的CCl4溶液中分离出碘 |
C、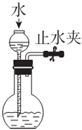 检查装置气密性 |
D、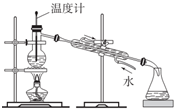 分离甲苯与乙醇 |
下列有关说法正确的是( )
| A、准确称取0.4000g NaOH固体可配成100mL 0.1000mol?L-1的NaOH标准溶液 |
| B、已知Ksp[Fe(OH)3]=4.0×10-38,则Fe3++3H2O?Fe(OH)3+3H+的平衡常数K=2.5×10-5 |
| C、100mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱 |
| D、对于反应2SO2(g)+O2(g)?2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |
 用下面三种方法均可制得Fe(OH)2白色沉淀.
用下面三种方法均可制得Fe(OH)2白色沉淀.