题目内容
下列有关摩尔的使用正确的是( )
| A、1mol O的质量为16g?mol-1 |
| B、0.5mol He约含有6.02×1023个电子 |
| C、2H既表示2个氢原子又表示2mol氢原子 |
| D、每摩尔微粒均含有6.02×1023个原子 |
考点:物质的量的单位--摩尔
专题:化学用语专题
分析:A、1molO的质量为16g;
B、He为单原子分子,每个He含有2个电子;
C、2H表示2个氢原子,不能表示2mol氢原子;
D、每摩尔微粒均含有6.02×1023个微粒.
B、He为单原子分子,每个He含有2个电子;
C、2H表示2个氢原子,不能表示2mol氢原子;
D、每摩尔微粒均含有6.02×1023个微粒.
解答:
解:A、1molO的质量为16g,故A错误;
B、He为单原子分子,0.5mol He约含有0.5×6.02×1023个原子,每个原子含有2个电子,因此电子数为2×0.5×6.02×1023=6.02×1023个,故B正确;
C、2H表示2个氢原子,不能表示2mol氢原子,故C错误;
D、每摩尔微粒均含有6.02×1023个微粒,由于微粒的组成不同,原子数不一定为6.02×1023个,故D错误;
故选B.
B、He为单原子分子,0.5mol He约含有0.5×6.02×1023个原子,每个原子含有2个电子,因此电子数为2×0.5×6.02×1023=6.02×1023个,故B正确;
C、2H表示2个氢原子,不能表示2mol氢原子,故C错误;
D、每摩尔微粒均含有6.02×1023个微粒,由于微粒的组成不同,原子数不一定为6.02×1023个,故D错误;
故选B.
点评:本题考查了物质的量的单位-摩尔、阿伏加德罗常数的定义,题目难度不大,注意阿伏加德罗常数的定义.

练习册系列答案
相关题目
Fe(OH)3胶体稳定存在的主要原因是( )
| A、胶粒直径小于1nm |
| B、胶粒做布朗运动 |
| C、胶粒带正电荷 |
| D、胶粒不能透过半透膜 |
氨能跟氧气在铂催化下反应生成硝酸和水,其中第一步反应为:4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(H2O)[mol?L-1?min-1]表示,则正确的关系是( )
| A、4v(NH3)=5v(O2) |
| B、5v(O2)=6v(H2O) |
| C、2v(NH3)=3v(H2O) |
| D、4v(O2)=5v(NO) |
氨氧化制硝酸,吸收塔内发生反应 3NO2(g)+H2O(l)?2HNO3(aq)+NO△H<0 要提高反应的转化率,增加浓硝酸的产量,应采取的措施( )
| A、加压 | B、加大水量 |
| C、升温 | D、减压 |
设NA代表阿伏加德罗常数的数值,下列说法不正确的是( )
| A、36g镁在足量的二氧化碳气体中完全燃烧共转移的电子数为3NA |
| B、1L 1mol?L-1的Na2CO3溶液中含有Na+的数目为NA |
| C、标准状况下,2.24L CO2和SO2混合气体中含有的氧原子数目为0.2NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
A、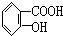 |
B、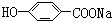 |
| C、H2NCH2COONa |
| D、Na2CO3 |
下列化学用语书写正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、丙烯的键线式: |
C、CH4分子的比例模型: |
D、乙醇的结构式: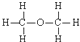 |