题目内容
根据表提供的数据,下列判断正确的是( )
| 酸 | 电离常数Ka |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| CH3COOH | Ka=1.8×10-5 |
| HClO | Ka=3.0×10-8 |
| A、pH相同的Na2CO3、CH3COONa、NaClO各加水稀释相同倍数,pH变化最小的是Na2CO3 |
| B、表中所列的三种酸的溶液中滴入石蕊试剂,溶液一定都变红 |
| C、次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=CO32-+2HClO |
| D、常温下,在0.1mol/L的CH3COOH溶液中滴加0.1mol/L的NaOH溶液发生反应,当c(H+)=1.8×10-5时,溶液中下列微粒的浓度大小关系为:c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:A.pH相同的Na2CO3、CH3COONa、NaClO,弱酸根离子水解程度越大,其浓度越小,所以这三种溶液浓度大小顺序是c(CH3COONa)>c(NaClO)>c(Na2CO3),加水稀释促进水解,稀释相同的倍数,酸越弱的钠盐溶液pH变化越小;
B.次氯酸具有漂白性;
C.次氯酸酸性大于碳酸氢根离子,次氯酸钠溶液中通入少量二氧化碳,二者反应生成次氯酸和碳酸氢钠;
D.常温下,二者混合,当c(H+)=1.8×10-5时,K(CH3COOH)=
,据此计算c(CH3COO-)、c(CH3COOH)相对大小.
B.次氯酸具有漂白性;
C.次氯酸酸性大于碳酸氢根离子,次氯酸钠溶液中通入少量二氧化碳,二者反应生成次氯酸和碳酸氢钠;
D.常温下,二者混合,当c(H+)=1.8×10-5时,K(CH3COOH)=
| c(CH3COO-).c(H+) |
| c(CH3COOH) |
解答:
解:A.pH相同的Na2CO3、CH3COONa、NaClO,弱酸根离子水解程度越大,其浓度越小,所以这三种溶液浓度大小顺序是c(CH3COONa)>c(NaClO)>c(Na2CO3),加水稀释促进水解,稀释相同的倍数,酸越弱的钠盐溶液pH变化越小,碳酸氢根离子酸性最弱,所以稀释相同的倍数时碳酸钠pH变化最小,故A正确;
B.这三种酸溶液都呈酸性,加入石蕊试剂后溶液呈红色,但次氯酸具有漂白性,所以次氯酸溶液使石蕊试液褪色,故B错误;
C.次氯酸钠溶液中通入少量二氧化碳,二者反应生成次氯酸和碳酸氢钠,离子方程式为ClO-+CO2+H2O=HCO3-+HClO,故C错误;
D.常温下,二者混合,当c(H+)=1.8×10-5时,K(CH3COOH)=
=
=1.8×10-5,所以c(CH3COO-)=c(CH3COOH),故D错误;
故选A.
B.这三种酸溶液都呈酸性,加入石蕊试剂后溶液呈红色,但次氯酸具有漂白性,所以次氯酸溶液使石蕊试液褪色,故B错误;
C.次氯酸钠溶液中通入少量二氧化碳,二者反应生成次氯酸和碳酸氢钠,离子方程式为ClO-+CO2+H2O=HCO3-+HClO,故C错误;
D.常温下,二者混合,当c(H+)=1.8×10-5时,K(CH3COOH)=
| c(CH3COO-).c(H+) |
| c(CH3COOH) |
| c(CH3COO-)×1.8×10-5 |
| c(CH3COOH) |
故选A.
点评:本题考查离子浓度大小比较、弱电解质电离及盐类水解,明确弱酸酸性强弱与酸根离子水解程度关系是解本题关键,注意次氯酸的漂白性,易错选项是D,会根据电离平衡常数确定醋酸和醋酸根离子浓度关系,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、CO2的相对分子质量为44g/mol |
| B、“物质的量”是“物质的质量”的简称 |
| C、摩尔只能用于计量纯净物 |
| D、阿伏伽德罗常数的单位是mol-1 |
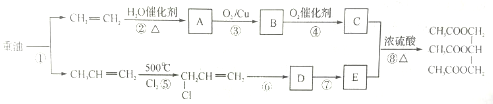

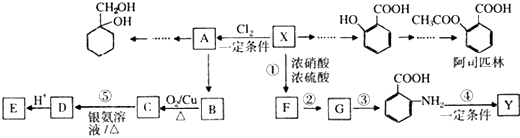
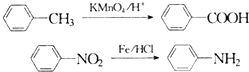 (苯胺,易被氧化)
(苯胺,易被氧化)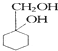 的流程图:
的流程图: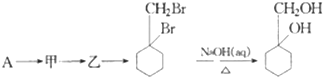
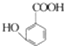 多一个碳原子的同系物M有多种同分异构体,同时符合下列4个条件的M同分异构体有
多一个碳原子的同系物M有多种同分异构体,同时符合下列4个条件的M同分异构体有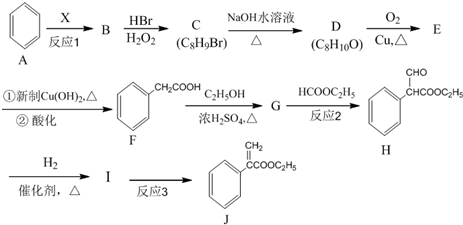
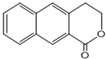 是一种重要的药物合成中间体,请结合题目所给信息,写出以
是一种重要的药物合成中间体,请结合题目所给信息,写出以 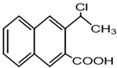 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2