题目内容
如图所示是一个制取氯气并以氯气为原料进行特定反应的装置,多余的氯气可以贮存在b瓶中,其中各试剂瓶中所装试剂为:B (水)、C (紫色石蕊试液)、D (碘化钾淀粉溶液)、F(烧碱溶液).
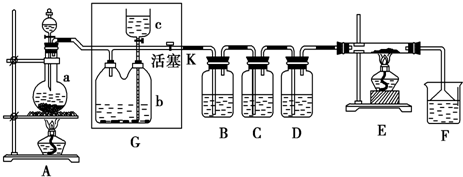
(1)反应完成后B中所得液体俗称 ;F装置的作用为 .
(2)实验开始后C中的现象是 ,D中的现象是 .
(3)E装置中硬质玻璃管内盛有铁粉,写出E中反应的化学方程式: .

(1)反应完成后B中所得液体俗称
(2)实验开始后C中的现象是
(3)E装置中硬质玻璃管内盛有铁粉,写出E中反应的化学方程式:
考点:实验装置综合,氯、溴、碘的性质实验
专题:实验题
分析:(1)B中为水,通入氯气形成氯水;氯气为有毒气体,要进行尾气处理;
(2)氯气溶于水生成HCl和HClO,根据二者的性质分析;氯气与碘化钾反应生成碘单质;
(3)Fe与氯气反应生成三氯化铁.
(2)氯气溶于水生成HCl和HClO,根据二者的性质分析;氯气与碘化钾反应生成碘单质;
(3)Fe与氯气反应生成三氯化铁.
解答:
解:(1)已知B中为水,A装置为氯气的发生装置,生成的氯气进入B中与水反应形成氯水;氯气为有毒气体,为了防止污染空气,要进行尾气处理,则F装置的作用是尾气处理,故答案为:氯水;尾气处理;
(2)氯气溶于水生成HCl和HClO,HCl有酸性使紫色石蕊试液,HClO具有漂白性使溶液褪色;氯气与碘化钾反应生成碘单质,碘与淀粉溶液在一起会变蓝色,
故答案为:试液先变红后褪色;溶液变蓝色;
(3)Fe与氯气在加热条件下反应生成三氯化铁,其反应的方程式为:2Fe+3Cl2
2FeCl3,故答案为:2Fe+3Cl2
2FeCl3.
(2)氯气溶于水生成HCl和HClO,HCl有酸性使紫色石蕊试液,HClO具有漂白性使溶液褪色;氯气与碘化钾反应生成碘单质,碘与淀粉溶液在一起会变蓝色,
故答案为:试液先变红后褪色;溶液变蓝色;
(3)Fe与氯气在加热条件下反应生成三氯化铁,其反应的方程式为:2Fe+3Cl2
| ||
| ||
点评:本题考查了实验室制备氯气的反应原理和装置选择,选择验证和反应现象判断,物质性质和实验基本操作是解题关键,题目难度不大.

练习册系列答案
相关题目
用电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变,且用惰性电极,下列说法不正确的是( )
| A、当电池负极消耗m g气体时,电解池阴极同时有m g气体生成 |
| B、电池的正极反应式为:O2+2H2O+4e-═4OH- |
| C、电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| D、燃料电池中c(KOH)不变 |
丙烯酸的结构简式为CH2=CH-COOH,对其性质的描述不正确的是( )
| A、能与金属钠反应放出氢气 |
| B、能发生加聚反应生成高分子化合物 |
| C、能与新制氢氧化铜反应 |
| D、能与溴水发生氧化反应使其褪色 |
 如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条看不到明显现象;关闭B阀后,C处红布逐渐褪色.则D瓶中装的是( )
如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条看不到明显现象;关闭B阀后,C处红布逐渐褪色.则D瓶中装的是( )| A、浓H2SO4 |
| B、NaOH溶液 |
| C、H2O |
| D、Na2S溶液 |
某浓度的氨水中存在下列平衡:NH3?H2O?NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,下列措施不正确的是( )
| A、加少量MgCl2 |
| B、加入NH4Cl固体 |
| C、适当升高温度 |
| D、加入少量盐酸 |
 如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.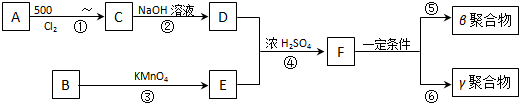
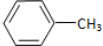
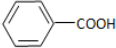
 ,
,