题目内容
14.在一个绝热的密闭反应容器中,只发生以下两个反应:M(g)+N(g)?2P(g)△H1<0
X(g)+3Y(g)?2Z(g)△H2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列说法中错误的是( )
| A. | 等压时,通入稀有气体He,反应容器中温度升高 | |
| B. | 等压时,通入Z气体,P气体的物质的量不变 | |
| C. | 等容时,通入稀有气体He,两个反应速率均不变 | |
| D. | 等容时,通入Z气体,Y的物质的量浓度增大 |
分析 A.等压时,绝热的密闭反应容器中通入稀有气体He,为保持压强不变,体积增大压强减小平衡X(g)+3Y(g)?2Z(g)逆向进行;
B.等压时,通入Z气体X(g)+3Y(g)?2Z(g)逆向进行,温度升高,则M(g)+N(g)?2P(g)平衡逆向进行,P气体的物质的量减小;
C.等容时通入稀有气体He,总压增大,气体分压不变,平衡不变,两个反应速率均不变;
D.等压时,通入Z气体X(g)+3Y(g)?2Z(g)逆向进行;
解答 解:A.等压时,绝热的密闭反应容器中通入稀有气体He,为保持压强不变,体积增大压强减小平衡X(g)+3Y(g)?2Z(g)逆向进行,逆向是放热反应,反应容器中温度升高,故A正确;
B.等压时,通入Z气体X(g)+3Y(g)?2Z(g)逆向进行,温度升高,则M(g)+N(g)?2P(g)平衡逆向进行,P气体的物质的量减小,故B错误;
C.等容时,绝热的密闭反应容器通入稀有气体He,总压增大,气体分压不变,平衡不变,两个反应速率均不变,故C正确;
D.等压时,通入Z气体X(g)+3Y(g)?2Z(g)逆向进行,Y的物质的量浓度增大,故D正确;
故选B.
点评 本题考查了恒温容器、恒压容器中改变条件对化学平衡的影响,注意是绝热的密闭反应容器,掌握化学平衡移动原理和反应特征,题目难度中等.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
3.下列说法不正确的是( )
| A. | 科学仪器的使用利于我们认识物质的微观世界,现在人们借助扫描隧道显微镜,应用STM技术可以“看”到越来越细微的结构,并实现对原子或分子的操纵 | |
| B. | 视频《穹顶之下》再次引起公众对“PM2.5”的关注.“PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 臭氧是一种有鱼腥味、氧化性极强的淡蓝色气体,可用作自来水的消毒剂 | |
| D. | 我国油品从国 IV 汽油升级到国 V 汽油,有助于减少酸雨、雾霾,提高空气质量 |
2.随着氮氧化物污染的日趋严重,国家将于“十三五”期间加大对氮氧化物排放的控制力度.目前,消除氮氧化物污染的方法有多种.
(1)用活性炭还原法处理氮氧化物.有关反应为C(s)+2NO(g)?(g)+CO2(g),某研究小组向某密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
①30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是降低N2的浓度.
②若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H<0(填“>”、“=”或“<”).
(2)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(I)△H=-44.0kJ•mol-1
写出CH4 (g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)△H=-955kJ•mol-1.
(3)①取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
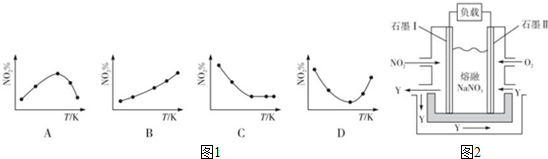
2NO2(g)?N2O4(g)△H<0.反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.下列示意图中如图1,可能与实验结果相符的是BD.
②保持温度、体积不变,向上述平衡体系中再通入一定量的NO2,则达平衡时NO2的转化率增大(填“增大”、“减小”、“不变”或“无法确定”).
③由NO2、O2、熔融NaNO3组成的燃料电池装置如图2所示,在使用过程中石墨I电极上发生反应生成一种氧化物Y,其电极反应式NO2+NO3--e-=N2O5.
(1)用活性炭还原法处理氮氧化物.有关反应为C(s)+2NO(g)?(g)+CO2(g),某研究小组向某密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| l0 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.017 | 0.034 |
| 50 | 0.032 | 0.017 | 0.034 |
②若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H<0(填“>”、“=”或“<”).
(2)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(I)△H=-44.0kJ•mol-1
写出CH4 (g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)△H=-955kJ•mol-1.
(3)①取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)?N2O4(g)△H<0.反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.下列示意图中如图1,可能与实验结果相符的是BD.

②保持温度、体积不变,向上述平衡体系中再通入一定量的NO2,则达平衡时NO2的转化率增大(填“增大”、“减小”、“不变”或“无法确定”).
③由NO2、O2、熔融NaNO3组成的燃料电池装置如图2所示,在使用过程中石墨I电极上发生反应生成一种氧化物Y,其电极反应式NO2+NO3--e-=N2O5.
19.下列关于有机物的说法正确的是( )
| A. | 无机物的种类比有机物多 | |
| B. | 互为同系物的有机物有可能同时互为同分异构体 | |
| C. | 丁烷有两种同分异构体 | |
| D. | 醇和醚均互为同分异构体 |
6.下列除杂所用的仪器方法,不正确的是( )
| A. | 苯中的甲苯:加溴水分液 | |
| B. | 乙醇中的水:加新制CaO蒸馏 | |
| C. | 甲烷中的乙烯:用溴的四氯化碳溶液洗气 | |
| D. | 乙酸乙酯中的乙酸:加饱和Na2CO3溶液分液 |
3.已知:0.1mol/LH2A溶液中c(H+)=0.11mol/L.
(1)写出H2A的第一步电离方程式H2A=H++HA-.
(2)0.1mol/LNaHA溶液中离子浓度从大到小的顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),其中c(H+)>0.01mol/L(填“>”、“=”或“<”),
(3)写出H2A溶液与过量NaOH溶液反应的离子方程式H++HA-+2OH-=A2-+2H2O
(4)已知:①上述四种酸中,酸性最强的是CH3COOH;
②25℃时,0.01mol/LNaCN溶液的pH>7;
③在浓度均为0.01mol/L的CH3COONa、NaC10、Na2C03的混合溶液中,逐滴加人0.01mo l/LHCl,则体系中酸根离子反应的先后顺序为CO32-、ClO-、HCO3-、CH3COO-.
(1)写出H2A的第一步电离方程式H2A=H++HA-.
(2)0.1mol/LNaHA溶液中离子浓度从大到小的顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),其中c(H+)>0.01mol/L(填“>”、“=”或“<”),
(3)写出H2A溶液与过量NaOH溶液反应的离子方程式H++HA-+2OH-=A2-+2H2O
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | HCN | 5×10-10 |
| H2CO3 | Ka1=4.2×10-7 | HClO | 3×10-8 |
| Ka2=5.6×10-11 |
②25℃时,0.01mol/LNaCN溶液的pH>7;
③在浓度均为0.01mol/L的CH3COONa、NaC10、Na2C03的混合溶液中,逐滴加人0.01mo l/LHCl,则体系中酸根离子反应的先后顺序为CO32-、ClO-、HCO3-、CH3COO-.
4.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为16.X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族.下列说法正确的是( )
| A. | 原子半径:r(Y)>r(Z) | |
| B. | X和Z都只能形成一种氧化物 | |
| C. | W的最高价氧化物对应的水化物是强酸 | |
| D. | Y的简单气态氢化物的热稳定性比W的弱 |
