题目内容
下列说法正确的是( )
| A、明矾[KAl(SO4)2?12H2O]溶解在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、玻璃具有耐腐蚀性,可以用玻璃试剂瓶长期保存酸、碱溶液 |
| C、浓H2SO4有强氧化性,但常温下可以用铁槽车运输 |
| D、将SO2通入溴水,溴水褪色后加热能恢复原色 |
考点:镁、铝的重要化合物,二氧化硫的化学性质,浓硫酸的性质,硅和二氧化硅
专题:元素及其化合物,化学应用
分析:A、明矾中的铝离子水解生成的氢氧化铝具有净水作用;
B、玻璃的主要成分二氧化硅可以和氢氟酸以及碱溶液之间发生反应;
C、常温下,金属铁遇到浓硫酸会发生钝化;
D、二氧化硫可以和溴水之间发生氧化还原反应产生无色溶液,据此回答.
B、玻璃的主要成分二氧化硅可以和氢氟酸以及碱溶液之间发生反应;
C、常温下,金属铁遇到浓硫酸会发生钝化;
D、二氧化硫可以和溴水之间发生氧化还原反应产生无色溶液,据此回答.
解答:
解:A、明矾中的铝离子水解生成形成Al(OH)3胶体,具有净水作用,所以明矾可用作净水剂,故A正确;
B、玻璃的主要成分二氧化硅可以和氢氟酸以及碱溶液之间发生反应,不可以用玻璃试剂瓶长期保存氢氟酸以及碱溶液,故B错误;
C、常温下,金属铁遇到浓硫酸会发生钝化,常温下可以用铁槽车运输浓硫酸,故C正确;
D、将SO2通入溴水,二氧化硫可以和溴水之间发生氧化还原反应产生氢溴酸和硫酸,得到了无色溶液,加热不能恢复原色,故D错误.
故选AC.
B、玻璃的主要成分二氧化硅可以和氢氟酸以及碱溶液之间发生反应,不可以用玻璃试剂瓶长期保存氢氟酸以及碱溶液,故B错误;
C、常温下,金属铁遇到浓硫酸会发生钝化,常温下可以用铁槽车运输浓硫酸,故C正确;
D、将SO2通入溴水,二氧化硫可以和溴水之间发生氧化还原反应产生氢溴酸和硫酸,得到了无色溶液,加热不能恢复原色,故D错误.
故选AC.
点评:本题考查学生物质的性质以及应用知识,是一道化学和实际联系的题目,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
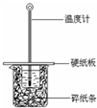 某实验小组用0.55mol/L NaOH溶液和0.50mol/L盐酸反应来测定中和热,实验装置如图所示.
某实验小组用0.55mol/L NaOH溶液和0.50mol/L盐酸反应来测定中和热,实验装置如图所示.
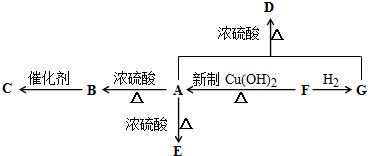
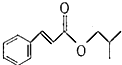 )是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下:
)是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下: