题目内容
6.(一)某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能;一是发生氧化还原反应:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;二是发生双水解反应:2Fe3++3SO32-+6H2O=2Fe2++2Fe(OH)3(胶体)+3H2SO4,为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:实验Ⅰ:学生选择的实验用品:Na2SO3浓溶液,BaCl2稀溶液,稀盐酸,试管若干,胶头滴管若干,从选择的药品分析,设计这个实验的目的是检验Na2SO3是否变质(或检验Na2SO3溶液中是否混有Na2SO4).
实验Ⅱ:取5mL FeCl3浓溶液于试管中,再滴加入 Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色,这种红褐色液体是氢氧化铁胶体向红褐色液体中加入稀盐酸至过量,将所得溶液分为两等份,其中一份加入KSCN溶液变成血红色,反应的离子方程式为Fe3++3SCN-=Fe(SCN)3.另一份加入BaCl2稀溶液有少量白色沉淀生成,产生该白色沉淀的离子方程式是Ba2++SO42-═BaSO4↓.
实验Ⅲ:换成两种稀溶液重复实验Ⅱ,产生现象完全相同,由上述实验得出的结论是Fe3+与SO32-同时发生氧化还原反应和双水解反应
若在FeCl3溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是2FeCl3+3Na2CO3+3H2O=2Fe(OH)3↓+3CO2↑+6NaCl.
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看出,二者的水溶液与FeCl3溶液反应现象差别很大,分析其可能的原因是:①SO32-有较强的还原性,CO32-没有还原性;②SO32-水解能力较CO32-小.
(二)镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.NiSO4•xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如下:
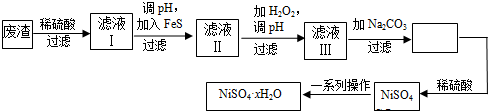
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为FeS(aq)+Cu2+(aq)=Fe2+(aq)+CuS(aq).
②滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是增大NiSO4浓度,富集Ni元素,有利于蒸发结晶.
分析 (一)实验Ⅰ:根据选择的实验用品“Na2SO3浓溶液、BaCl2稀溶液、稀盐酸”分析实验的目的;
实验Ⅱ:根据氢氧化铁的颜色为红褐色进行判断反应生成了氢氧化铁胶体;
加入KSCN溶液,溶液变为血红色,证明溶液中存在铁离子,另一份加入BaCl2稀溶液有少量白色沉淀生成是硫酸根离子结合钡离子形成硫酸钡沉淀的反应;
实验Ⅲ:根据反应生成了氢氧化铁和硫酸根离子进行分析;
根据碳酸根离子与铁离子发生了双水解生成氢氧化铁和二氧化碳写出离子方程式;
根据碳酸钠和亚硫酸钠的本身性质进行判断;
(二)电镀废渣(除镍外,还含有铜、锌、铁等元素),过滤后在滤液中加入FeS,生成CuS、ZnS,可除去Cu2+、Zn2+等杂质,对滤液Ⅱ先加W,应为过氧化氢,可氧化Fe2+生成Fe3+,有利于水解生成氢氧化铁沉淀而除去,过滤后在滤液中加入碳酸钠,可生成NiCO3,过滤后加入硫酸可生成NiSO4,经蒸发、浓缩、冷却结晶可得到硫酸镍晶体,以此解答.
解答 解:实验Ⅰ:学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸,目的是检验亚硫酸钠是否被氧化成了硫酸钠,
故答案为:检验Na2SO3是否变质(或检验Na2SO3溶液中是否混有Na2SO4);
实验Ⅱ:FeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,铁离子能够与亚硫酸根离子发生水解生成了红褐色的氢氧化铁胶体;
加入KSCN溶液,溶液变为血红色,反应反应的离子方程式为:Fe3++3SCN-═Fe(SCN)3,另一份加入BaCl2稀溶液有少量白色沉淀生成,产生该白色沉淀的离子方程式是:Ba2++SO42-═BaSO4↓,
故答案为:氢氧化铁胶体;Fe3++3SCN-=Fe(SCN)3; Ba2++SO42-═BaSO4↓;
实验Ⅲ:换用稀释的FeCl3和Na2SO3溶液重复实验Ⅱ,产生的现象完全相同,证明了Fe3+与SO32-发生氧化还原反应和双水解反应是同时进行的,
在FeCl3浓溶液中加Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,二者发生了双水解反应,反应的化学方程式为:2FeCl3+3Na2CO3+3H2O=2Fe(OH)3↓+3CO2↑+6NaCl;
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看出,二者的水溶液与FeCl3溶液反应现象差别很大,分析其可能的原因是:
由于亚硫酸根离子具有较强的还原性,能够与铁离子发生氧化还原反应,而碳酸根离子没有还原性;
铁离子与亚硫酸根离子生成了氢氧化铁胶体,与碳酸根离子反应生成了氢氧化铁沉淀,说明碳酸根离子水解能力比亚硫酸根离子大,
故答案为:Fe3+与SO32-同时发生氧化还原反应和双水解反应;2FeCl3+3Na2CO3+3H2O=2Fe(OH)3↓+3CO2↑+6NaCl;SO32-有较强的还原性,CO32-没有还原性;SO32-水解能力较CO32-小;
(二)电镀废渣(除镍外,还含有铜、锌、铁等元素),过滤后在滤液中加入FeS,生成CuS、ZnS,可除去Cu2+、Zn2+等杂质,对滤液Ⅱ先加W,应为过氧化氢,可氧化Fe2+生成Fe3+,有利于水解生成氢氧化铁沉淀而除去,过滤后在滤液中加入碳酸钠,可生成NiCO3,过滤后加入硫酸可生成NiSO4,经蒸发、浓缩、冷却结晶可得到硫酸镍晶体,
①向滤液Ⅰ中加入FeS主要目的是除去Cu、Zn等杂质,说明CuS的溶解度更小,反应的离子方程式为FeS(aq)+Cu2+(aq)=Fe2+(aq)+CuS(aq),
故答案为:FeS(aq)+Cu2+(aq)=Fe2+(aq)+CuS(aq);
②滤液Ⅲ溶质的主要成分是NiSO4,再加入碳酸钠过滤后,加稀硫酸溶解又生成NiSO4,可增大成NiSO4浓度,有利于蒸发结晶,
故答案为:增大NiSO4浓度,富集Ni元素,有利于蒸发结晶.
点评 本题考查了探究反应机理的方法,铝的重要化合物性质、电离方程式、离子方程式的书写,题目难度中等,注意掌握常见元素单质及其化合物性质,明确离子方程式、电离方程式的书写原则,本题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案| A. | 与Al反应能放出H2的溶液中可能大量存在Fe2+、Na+、NO3-、Cl- | |
| B. | 使紫色石蕊变蓝的溶液中可能大量存在Al3+、SO42-、NH4+、CO32- | |
| C. | Al2(SO4)3溶液与氨水的反应:Al3++3OH-=Al(OH)3↓ | |
| D. | FeCl3溶液腐蚀印刷电路板的反应:2Fe3++Cu=2Fe2++Cu2+ |
| A. | 明矾净水原理不涉及化学变化 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”的还原性比铜片更强 |
| A. | 8种 | B. | 10种 | C. | 16种 | D. | 20种 |
| A. | 1 mol的CH4质量为16g/mol | |
| B. | 3.01×1023个CO2分子的质量约为22g | |
| C. | H2O的摩尔质量为18g | |
| D. | 标准状况下,1 mol任何物质体积均为22.4L |
| A. | 处理废水中Cr2O72- 的物质量为$\frac{nx}{2}$mol | |
| B. | 消耗绿矾的物质量为n(2-x)mol | |
| C. | 反应中发生转移的电子数为3nx mol | |
| D. | 反应中Cr2O72-被还原 |
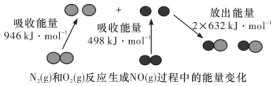 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 在1 L的容器中发生反应,10 min内 N2 减少了1 mol,因此10 min内的平均反应速率为v(NO)=0.1 mol/(L•min) | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
 .
.