题目内容
3.下列关于浓硫酸的叙述中,正确的是( )| A. | 常温时与锌反应生成大量氢气 | |
| B. | 置于敞口容器中,经过一段时间后质量将减少 | |
| C. | 常温时与铁、铝不反应 | |
| D. | 稀释时将浓硫酸沿器壁慢慢加到水中并不断搅拌 |
分析 A.浓硫酸具有强氧化性,与金属反应不产生氢气;
B.依据浓硫酸具有吸水性解答;
C.浓硫酸具有强氧化性,常温下遇到铁、铝钝化;
D.依据浓硫酸稀释的正确操作解答.
解答 解:A.浓硫酸具有强氧化性,与金属反应不产生氢气,故A错误;
B.浓硫酸具有吸水性,置于敞口容器中,经过一段时间后质量将增加,故B错误;
C.浓硫酸具有强氧化性,常温下遇到铁、铝钝化,钝化属于化学反应,故C错误;
D.稀释浓硫酸时应将浓硫酸沿器壁慢慢地注入水中,并不断搅拌,切不可把水倒入浓硫酸中,故D正确;
故选:D.
点评 本题考查了浓硫酸的性质,熟悉浓硫酸的吸水性、强氧化性是解题关键,注意浓硫酸使铁、铝钝化属于化学变化,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
7.如表各组物质中,不能按a→b→c关系相互转化的是(“→”表示一步完成)( )
| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | Na | Na2O2 | NaOH |
| C | Si | SiO2 | H2SiO3 |
| D | HNO3 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
8.三草酸合铁(Ⅲ)酸钾晶体(Kx[Fey(C2O4)Z]•nH2O)可用于摄影,为确定其组成进行如下实验:
步骤1:准确称取该晶体0.9820g,配成溶液,平均分成10份.
步骤2:取一份溶液,酸化,加热,用SnCl2-TiCl3将Fe3+全部还原为Fe2+,再加0.0100mol•L-1KMnO4至恰好反应,将C2O42-全部氧化成CO2,Fe2+全部氧化成Fe3+,消耗KMnO4体积28.00mL.
步骤3:另取一份溶液,酸化,加入0.0100mol•L-1KMnO4至恰好反应完全,将C2O42-全部氧化成CO2,消耗KMnO4体积24.00mL.
(已知:MnO${\;}_{4}^{-}$还原产物为Mn2+,上述实验数据为多次实验有效数据平均值)
下列判断正确的是( )
步骤1:准确称取该晶体0.9820g,配成溶液,平均分成10份.
步骤2:取一份溶液,酸化,加热,用SnCl2-TiCl3将Fe3+全部还原为Fe2+,再加0.0100mol•L-1KMnO4至恰好反应,将C2O42-全部氧化成CO2,Fe2+全部氧化成Fe3+,消耗KMnO4体积28.00mL.
步骤3:另取一份溶液,酸化,加入0.0100mol•L-1KMnO4至恰好反应完全,将C2O42-全部氧化成CO2,消耗KMnO4体积24.00mL.
(已知:MnO${\;}_{4}^{-}$还原产物为Mn2+,上述实验数据为多次实验有效数据平均值)
下列判断正确的是( )
| A. | 取溶解后待测液少许,先加少量氯水,再加KSCN产生血红色溶液,则有Fe2+ | |
| B. | 步骤3的离子方程式为:5C2O42-+2MnO${\;}_{4}^{-}$+8H2O=10CO2↑+2Mn2++16OH- | |
| C. | x:z=1:2 | |
| D. | 该晶体的化学式为:K3[Fe(C2O4)3]•3H2O |
11.价层电子对互斥理论(简称VSEPR理论)可用于预测简单分子的立体构型.其要点可以概括为:
Ⅰ.用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间;
Ⅱ.分子的空间构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为:
ⅰ.孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ.双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ.X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强;ⅳ.其他.请仔细阅读上述材料,回答下列问题:
(1)根据要点Ⅰ可以画出AXnEm的VSEPR理想模型,请填写下表:
(2)请用VSEPR模型解释CO2为直线形分子的原因:CO2属AX2E0,n+m=2,故为直线形;
(3)用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型:
Ⅰ.用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间;
Ⅱ.分子的空间构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为:
ⅰ.孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ.双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ.X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强;ⅳ.其他.请仔细阅读上述材料,回答下列问题:
(1)根据要点Ⅰ可以画出AXnEm的VSEPR理想模型,请填写下表:
| n+m | 2 | |
| VSEPR理想模型 | 正四面体形 | |
| 价层电子对 之间的理想键角 | 109°28′ |
(3)用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型:
| 分子 | |||
| 或离子 | SnCl2 | CCl4 | ClO${\;}_{4}^{-}$ |
| 立体构型 |
18.1L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol/L和2b mol/L,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用( )
| A. | Ca(OH)2 | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
8.下列反应中,符合能量变化如图所示的反应是( )
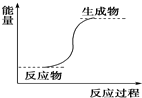

| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸 | ||
| C. | NaOH与HCl的反应 | D. | 甲烷与O2的燃烧反应 |
15.①正丁烷 ②2-甲基丙烷 ③正戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷等物质沸点的排列顺序正确的是( )
| A. | ①>②>③>④>⑤ | B. | ②>①>⑤>④>③ | C. | ③>④>⑤>①>② | D. | ⑤>④>③>②>① |
12.电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法正确的是( )
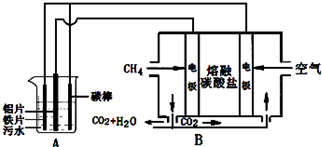

| A. | 装置A中碳棒为阴极 | |
| B. | 污水中加入适量的硫酸钠,可增强溶液的导电性 | |
| C. | 装置B中通入空气的电极反应是O2+2H2O+4e-=4OH- | |
| D. | 标准状况下,若A装置中产生44.8 L气体,则理论上B装置中要消耗CH411.2L |
13.下列事实与其对应的方程式解释均正确的是( )
| A. | 用惰性电极电解MgCl2 溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 1molN2与3molH2在某密闭容器中反应放出73kJ热量,则反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-73kJ/mol | |
| C. | 将AlCl3溶液与Na2S混合产生沉淀:2Al3++3S2-═Al2S3↓ | |
| D. | 2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-akJ•mol-1,则中和热为0.5akJ•mol-1 |