题目内容
经测定0.1mol/L的KHSO4溶液与0.1mol/L的HCl溶液中的氢离子浓度基本相同,则:
(1)KHSO4的电离方程式可以表示为
(2)往0.1mol/L的KHSO4溶液中加入锌片,预计可以观察到的现象是 ,反应的离子方程式为 .
(3)某同学向一定量的KHSO4溶液中滴加Ba(OH)2溶液至混合液呈中性,此时的变化可以用离子方程式表示为 ,继续滴加Ba(OH)2溶液,其变化可以用离子方程式表示为 .
(1)KHSO4的电离方程式可以表示为
(2)往0.1mol/L的KHSO4溶液中加入锌片,预计可以观察到的现象是
(3)某同学向一定量的KHSO4溶液中滴加Ba(OH)2溶液至混合液呈中性,此时的变化可以用离子方程式表示为
考点:离子方程式的书写
专题:离子反应专题
分析:(1)强电解质,完全电离生成钠离子、氢离子和硫酸根离子;
(2)KHSO4溶液中加入锌片,Zn与氢离子反应生成氢气;
(3)至混合液呈中性,以2:1反应生成硫酸钡、硫酸钾和水;继续滴加Ba(OH)2溶液,硫酸钾与钡离子反应生成硫酸钡沉淀.
(2)KHSO4溶液中加入锌片,Zn与氢离子反应生成氢气;
(3)至混合液呈中性,以2:1反应生成硫酸钡、硫酸钾和水;继续滴加Ba(OH)2溶液,硫酸钾与钡离子反应生成硫酸钡沉淀.
解答:
解:(1)强电解质,完全电离生成钠离子、氢离子和硫酸根离子,电离方程式为KHSO4=K++H++SO42-,故答案为:KHSO4=K++H++SO42-;
(2)KHSO4溶液中加入锌片,Zn与氢离子反应生成氢气,离子反应为Zn+2H+=Zn2++H2↑,观察到有无色气泡冒出,
故答案为:有无色气泡冒出;Zn+2H+=Zn2++H2↑;
(3)至混合液呈中性,以2:1反应生成硫酸钡、硫酸钾和水,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,继续滴加Ba(OH)2溶液,硫酸钾与钡离子反应生成硫酸钡沉淀,离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;Ba2++SO42-=BaSO4↓.
(2)KHSO4溶液中加入锌片,Zn与氢离子反应生成氢气,离子反应为Zn+2H+=Zn2++H2↑,观察到有无色气泡冒出,
故答案为:有无色气泡冒出;Zn+2H+=Zn2++H2↑;
(3)至混合液呈中性,以2:1反应生成硫酸钡、硫酸钾和水,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,继续滴加Ba(OH)2溶液,硫酸钾与钡离子反应生成硫酸钡沉淀,离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;Ba2++SO42-=BaSO4↓.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应及与量有关的离子反应考查,题目难度不大.

练习册系列答案
相关题目
2013年1月28日日本岛发生火山喷发,将滚热的云状火山气体和火山灰喷向高空.火山气体主要包括①水蒸气②CO2③SO2④SO3⑤HCl,这些气体对环境造成了极大的危害,对①~⑤中的相关气体的叙述中不正确的是( )
| A、收集一定量的火山气体通入足量BaCl2溶液中,只能生成BaSO4一种沉淀 |
| B、②③④属于酸性氧化物 |
| C、⑤属于强电解质 |
| D、①②③④属于非电解质 |
如图实验装置或操作与微粒的大小无直接关系的是( )
A、 过滤 |
B、 渗析 |
C、 萃取 |
D、 丁达尔效应 |
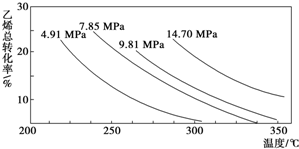 工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )| A、合成乙醇的反应一定为放热反应 |
| B、目前工业上采用250~300℃,主要是因为在此温度下乙烯的转化率最大 |
| C、目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率 |
| D、相同催化剂下,在300℃14.70 MPa乙醇产率反而比300℃7.85 MPa低得多,是因为加压平衡向逆反应方向移动 |
近年来我国大部分地区常被雾霾笼罩,PM2.5数据持续“爆表”,严重影响人们的身体健康.PM2.5是指大气中直径小于或等于2.5 μm(微米)的细小颗粒物,也称为可入肺颗粒物,它是大气的一种污染物,主要来自化石燃料的燃烧等.下列有关说法不正确的是( )
| A、“雾霾”不属于自然现象 |
| B、PM2.5的产生与人类活动有关 |
| C、PM2.5分散在空气中形成的混合物具有丁达尔效应 |
| D、开发利用新能源,减少化石燃料的使用是缓解雾霾天气发生的重要措施 |