题目内容
5.据报道,结构式为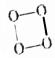 的O4是一种价格超过黄金的气体,下列有关O4的说法中不正确的是( )
的O4是一种价格超过黄金的气体,下列有关O4的说法中不正确的是( )| A. | O4与O3、O2互为同素异形体 | |
| B. | O4与H2反应生成冰 | |
| C. | O4中各原子最外电子层均达到8电子结构 | |
| D. | O4的化学性质一定比O2稳定 |
分析 根据结构式可知,1mol1molO4中含有4NA个O-O键,同种元素之间形成非极性共价键,O4为氧元素的单质,
A.同种元素组成的不同单质为同素异形体;
B.O4与H2反应是单质化合反应;
C.氧原子最外层6个电子,可以形成两个共价键达到8电子稳定结构;
D.O4是一种新型的氧分子,其化学性质比较活泼.
解答 解:A.O4与O3、O2是氧元素组成的不同单质为氧元素的同素异形体,故A正确;
B.O4与H2反应是单质化合反应生成冰,故B正确;
C.O4中氧原子最外层6个电子,可以形成两个共价键达到8电子稳定结构,各原子最外电子层均达到8电子结构,故C正确;
D.空气中有O2,没有O4,O4的化学性质比O2活泼,故D错误;
故选D.
点评 本题以信息的形式考查化学键,同素异形体,明确信息中的结构式是解答本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列说法不正确的是( )
| A. | NH4Cl溶液呈酸性说明NH3•H2O是弱电解质 | |
| B. | 醋酸钠溶液中c(Na+)>c(CH3COO-) | |
| C. | 常温下相同pH的NaOH溶液和CH3COONa溶液中水电离出的OH-浓度相同 | |
| D. | 常温下,在1mol•L-1的盐酸中加入等体积等浓度的氨水,溶液导电能力减弱 |
16.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将一定量的NaNO3和KCl混合加热浓缩至有固体析出,过滤. | 有白色晶体析出 | 白色晶体为KNO3 |
| B | 向2mLNaCl和NaI(浓度均为0.1mol•L-1)混合溶液中滴入2滴0.1mol•L-1AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向某溶液中加入盐酸酸化的Ba(NO3)2溶液 | 出现白色沉淀 | 该溶液一定有SO42-或 Ag+ |
| D | 向淀粉水解液中加入新制的Cu(OH)2悬浊液,煮沸 | 没有生成(砖)红色沉淀 | 淀粉未水解 |
| A. | A | B. | B | C. | C | D. | D |
13.常温常压下,下列各组气体不能共存的是( )
| A. | N2和O2 | B. | NO和O2 | C. | NO和NO2 | D. | NO2和O2 |
20.实验室需要用480mL 0.1mol•L-1的硫酸铜溶液,以下配制方法正确的是( )
| A. | 称取12.5 g胆矾(CuSO4•5H2O),配成500 mL溶液 | |
| B. | 称取12.5 g胆矾(CuSO4•5H2O),加入500 mL水配成溶液 | |
| C. | 称取7.68 g无水硫酸铜粉末,加入480 mL水配成溶液 | |
| D. | 称取8.0 g无水硫酸铜粉末,加入500 mL水配成溶液 |
10.标准状况下,下列物质中,其体积最大的是( )
| A. | 44g CO2 | B. | 11.2L H2 | C. | 2mol Fe | D. | 2mol H2O |
17.Cu和浓H2SO4反应得到25gCuSO4•5H2O,被还原的H2SO4是( )
| A. | 4.9g | B. | 8.0g | C. | 9.8g | D. | 19.6g |
15.设 NA 为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,28 g CO 和 C2H4混合气体中的碳原子数为 NA | |
| B. | 1 mol N2 与 3 mol H2 充分反应,产物的分子数为 2NA | |
| C. | 标准状况下,11.2 L 己烷中含有的碳碳键数为 2.5NA | |
| D. | 32 g 硫粉与足量的 Cu 粉完全反应,转移的电子数为 2NA |
 .
.