题目内容
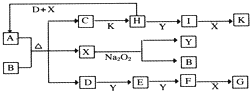
如图的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.试回答下列问题:
(1)D的电子式为: ;
(2)写出D+H+X→A的化学方程式: ;
(3)写出C→H的离子方程式: ;
(4)写出组成单质Y元素基态原子电子排布式为: .

(1)D的电子式为:
(2)写出D+H+X→A的化学方程式:
(3)写出C→H的离子方程式:
(4)写出组成单质Y元素基态原子电子排布式为:
考点:无机物的推断
专题:推断题
分析:X为无色液体,与过氧化钠反应得到B与气体Y,则X是H2O,Y是O2,B是NaOH.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,说明H应该是SO2.SO2具有还原性,被过氧化钠氧化生成硫酸钠,硫酸钠和钡离子反应生成硫酸钡白色沉淀.SO2被氧气氧化生成三氧化硫,三氧化硫溶于水生成硫酸,即I是SO3,K是H2SO4.一个D分子中含有10个电子,经过系列反应得到强酸G,则D是NH3,则E是NO,F是NO2,所以G是HNO3.A是由短周期元素组成的酸式盐,所以A是NH4HSO3,则C是Na2SO3,据此解答.
解答:
解:X为无色液体,与过氧化钠反应得到B与气体Y,则X是H2O,Y是O2,B是NaOH.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,说明H应该是SO2.SO2具有还原性,被过氧化钠氧化生成硫酸钠,硫酸钠和钡离子反应生成硫酸钡白色沉淀.SO2被氧气氧化生成三氧化硫,三氧化硫溶于水生成硫酸,即I是SO3,K是H2SO4.一个D分子中含有10个电子,经过系列反应得到强酸G,则D是NH3,则E是NO,F是NO2,所以G是HNO3.A是由短周期元素组成的酸式盐,所以A是NH4HSO3,则C是Na2SO3,
(1)D为NH3,电子式为: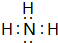 ,故答案为:
,故答案为: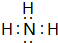 ;
;
(2)D+H+X→A的化学方程式为:SO2+NH3+H2O=NH4HSO3,故答案为:SO2+NH3+H2O=NH4HSO3;
(3)C→H的离子方程式为:SO32-+2H+=SO2↑+H2O,故答案为:SO32-+2H+=SO2↑+H2O;
(4)组成单质Y元素为氧元素,其基态原子电子排布式为:1S22S22P4,故答案为:1S22S22P4.
(1)D为NH3,电子式为:
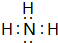 ,故答案为:
,故答案为: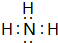 ;
;(2)D+H+X→A的化学方程式为:SO2+NH3+H2O=NH4HSO3,故答案为:SO2+NH3+H2O=NH4HSO3;
(3)C→H的离子方程式为:SO32-+2H+=SO2↑+H2O,故答案为:SO32-+2H+=SO2↑+H2O;
(4)组成单质Y元素为氧元素,其基态原子电子排布式为:1S22S22P4,故答案为:1S22S22P4.
点评:本题考查无机物推断,难度中等,需要学生熟练掌握元素化合物知识,注意根据转化关系中特殊反应进行推断.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、7.8 g Na2O2与足量潮湿的CO2反应,转移的电子数为0.1 NA |
| B、标准状况下2.24 L HCHO中含0.4 NA个原子 |
C、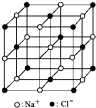 23.4 g NaCl晶体中含0.1 NA个如图所示结构单元 23.4 g NaCl晶体中含0.1 NA个如图所示结构单元 |
| D、电解精炼铜时转移0.1 NA个电子时,阳极溶解3.2 g铜 |
下列涉及有机物的说法正确的是( )
| A、新制氢氧化铜悬浊液可以鉴别乙酸溶液、葡萄糖溶液、淀粉溶液 |
| B、乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 |
| C、煤的干馏、石油的分馏都只发生了化学变化 |
| D、棉、麻、丝、毛完全燃烧都只生成CO2和H2O |
下列各组离子或分子,在溶液中不能大量共存的是( )
| A、NH4+、NO3-、HSO3-、NH3?H2O |
| B、K+、Al3+、SO42-、AlO2- |
| C、Na+、Fe3+、NO3-、MnO4- |
| D、Na+、CH3COO-、CO32-、HCO3- |
已知:95℃时,KW=1.0×10-12.在该温度下,测得0.1mol?L-1Na2A溶液pH=6,则下列说法正确的是( )
| A、H2A在水溶液中的电离方程式为:H2A?H++HA-,HA-?H++A2- |
| B、(NH4)2A溶液中存在离子浓度关系:c(NH4+)>c(A2-)>c(H+)>c(OH-) |
| C、0.0lmol?L-l的H2A溶液pH=2 |
| D、等体积等浓度的盐酸与H2A溶液分别与5.6g Zn反应,H2A溶液产生的H2多 |
已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数
CH3COOH?CH3COO-+H+ K1=1.75×10-5 △H1>0
CH3COO-+H2O+?CH3COOH+OH- K2=5.71×10-10 △H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是( )
CH3COOH?CH3COO-+H+ K1=1.75×10-5 △H1>0
CH3COO-+H2O+?CH3COOH+OH- K2=5.71×10-10 △H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是( )
| A、混合溶液PH<7 |
| B、对混合溶液进行微热,K1增大、K2减小 |
| C、调节混合溶液的PH值至中性,则此时溶液中c(Na+)═c(CH3COO-) |
| D、温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO-)减小 |
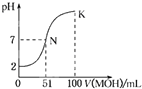 常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述正确的是( )
常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述正确的是( )| A、HA为弱酸,MOH为强碱 |
| B、pH=7时,HA与MOH恰好完全反应 |
| C、在N点,c(A-)═c(M+)+c(MOH) |
| D、在K点,c(M+)>c(A-)>c(OH-)>c(H+) |
下列物质属于含有共价键的离子化合物的是( )
| A、SiO2 |
| B、Na2O |
| C、Ca(OH)2 |
| D、H2SO4 |
 .
.