题目内容
在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)?cC(g)+dD(g) 达到平衡后,测得C气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积缩小为
,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
| 1 |
| 2 |
| A、反应速率降低 |
| B、平衡向右移动 |
| C、B的转化率提高 |
| D、a+b<c+d |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:保持温度不变,将容器的体积缩小1倍,如平衡不移动,C气体的浓度为1mol/L,实际C的浓度变为0.9mol/L,说明平衡向逆反应方向移动,据此结合选项解答.
解答:
解:保持温度不变,将容器的体积缩小1倍,如平衡不移动,C气体的浓度为1mol/L,实际C的浓度变为0.9mol/L,说明平衡向逆反应方向移动;
A、增大压强反应速率加快,故A错误;
B、保持温度不变,将容器的体积缩小1倍,如平衡不移动,C气体的浓度为1mol/L,实际C的浓度变为0.9mol/L,说明平衡向逆反应方向移动,故B错误;
C、平衡逆向移动,反反应物转化率降低,故C错误;
D、保持温度不变,将容器的体积缩小1倍,平衡向逆反应方向移动,说明反应物气体物质的量比生成物小,a+b<c+d,故D正确;
故选D.
A、增大压强反应速率加快,故A错误;
B、保持温度不变,将容器的体积缩小1倍,如平衡不移动,C气体的浓度为1mol/L,实际C的浓度变为0.9mol/L,说明平衡向逆反应方向移动,故B错误;
C、平衡逆向移动,反反应物转化率降低,故C错误;
D、保持温度不变,将容器的体积缩小1倍,平衡向逆反应方向移动,说明反应物气体物质的量比生成物小,a+b<c+d,故D正确;
故选D.
点评:本题考查学生影响化学平衡移动的因素等方面的知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列化学方程式中,可以用离子方程式 H++OH-═H2O表示的是( )
| A、3HCl+Fe(OH)3═FeCl3+3H2O |
| B、HNO3+KOH═KNO3+H2O |
| C、H2SO4+Ba(OH)2═BaSO4↓+2H2O |
| D、2HCl+Cu(OH)2═CuCl2+2H2O |
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
下列有关说法正确的是( )
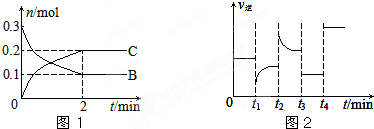
下列有关说法正确的是( )

| A、x=2,反应开始2 min内,v(B)=0.1 mol/(L?min) |
| B、t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 |
| C、t2时改变的条件可能是增大c(C),B的转化率增大 |
| D、t1时改变的条件可能是降温,A(s)的质量增加 |
向FeCl3和CuCl2混合液中加入过量的铁粉,反应完毕后,剩下的固体物质恰好跟加入的铁粉质量相等,则原混合液中FeCl3和CuCl2物质的量之比为( )
| A、2:7 | B、7:2 |
| C、1:7 | D、7:1 |
一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g.原混合气体中CO2的质量为( )
| A、12.5g |
| B、13.2g |
| C、19.7g |
| D、24.4g |

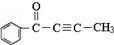 的有机物分子中:在同一直线上的碳原子最多有
的有机物分子中:在同一直线上的碳原子最多有