题目内容
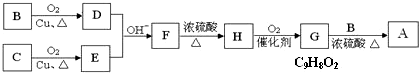
1.紫外线吸收剂BAD是天津合成材料研究所与天津市有机化工一厂合作研制的项目.利用芳香烃X和链烃Y可以合成紫外线吸收剂BAD,已知G不能发生银镜反应.BAD的合成路线如下: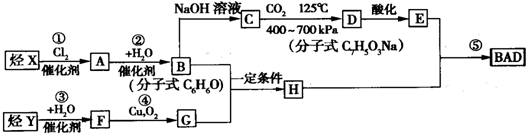
BAD的结构简式为:

已知双酚H可以采用苯酚与丙酮在酸性条件下催化缩合而成:
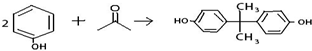
试回答下列问题:
(1)写出结构简式:YCH3CH=CH2;D
 .
.(2)属于取代反应的有①②⑤(填数字序号).
(3)1mol BAD最多可与含6mol NaOH的溶液完全反应.
(4)写出下列反应的化学方程式:
反应④:
 ;
;E+H→BAD2
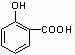 +
+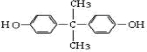 →
→ +2H2O.(不须写反应条件)
+2H2O.(不须写反应条件)
分析 由BAD结构简式可知E为 ,H为
,H为 ,根据D的分子式结合E的结构可知D为
,根据D的分子式结合E的结构可知D为 ,根据B的分子式可知B为
,根据B的分子式可知B为 ,则A为
,则A为 ,烃X为苯,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,应为酮,结合B和H的结构可知G为
,烃X为苯,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,应为酮,结合B和H的结构可知G为 ,则F为CH3CHOHCH3,烃Y为CH3CH=CH2,结合有机物的结构和性质解答该题.
,则F为CH3CHOHCH3,烃Y为CH3CH=CH2,结合有机物的结构和性质解答该题.
解答 解:由BAD结构简式可知E为 ,H为
,H为 ,根据D的分子式结合E的结构可知D为
,根据D的分子式结合E的结构可知D为 ,根据B的分子式可知B为
,根据B的分子式可知B为 ,则A为
,则A为 ,烃X为苯,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,应为酮,结合B和H的结构可知G为
,烃X为苯,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,应为酮,结合B和H的结构可知G为 ,则F为CH3CHOHCH3,烃Y为CH3CH=CH2,
,则F为CH3CHOHCH3,烃Y为CH3CH=CH2,
(1)由以上分子可知Y为CH3CH=CH2,D为 ,故答案为:CH3CH=CH2;
,故答案为:CH3CH=CH2; ;
;
(2)由转化关系可知①为取代反应,②为取代反应,③为加成反应,④为氧化反应,⑤为取代反应,
故答案为:①②⑤;
(3)根据BAD结构简式可知,BAD水解生成4个酚羟基和2个羧基,则1molBAD最多可与含6molNaOH的溶液反应,
故答案为:6;
(4)④的反应方程式为: ,
,
由官能团的变化可知E+H→BAD反应为取代反应,方程式为2 +
+ →
→ +2H2O,
+2H2O,
故答案为: ,2
,2 +
+ →
→ +2H2O.
+2H2O.
点评 本题考查有机化学中的框图题,属中档题,题目可以采用正、逆两种方式同时进行推断.剖析BAD可知,其中含有苯酚的结构,因此可推断B为苯酚,以此为突破口进行推断,注意把握有机物官能团的性质和变化,答题时要仔细审题.

练习册系列答案
相关题目
12.10℃时加热饱和NaHCO3溶液,测得该溶液的pH发生如表所示的变化.
甲同学认为,该溶液pH增大的原因是HCO3-的水解程度增大,故碱性增强,有关反应的离子方程式为HCO3-+H2O?H2CO3+OH-.乙同学认为,溶液pH增大的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3的水解程度,该分解反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.丙同学认为,甲、乙的判断都不充分,他进行如下探究来验证他们的判断是否正确.
(1)在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确,试剂X是B(填序号).
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH=8.3,则甲(填“甲”或“乙”)的判断正确.
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确,试剂X是B(填序号).
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH=8.3,则甲(填“甲”或“乙”)的判断正确.
9.有X、Y、Z、W、M五种原子序数依次增大的短周期元素,其中X、M同主族;Z+与Y2-具有相同的电子层结构,W是地壳中含量最多的金属,X与W的原子序数之和等于Y与Z的原子序数之和.下列说法不正确的是( )
| A. | 离子半径大小:r(Y 2-)>r(Z +)>r(W 3+) | |
| B. | W的氧化物对应的水化物可能与Z的最高价氧化物的水化物反应 | |
| C. | X有多种同素异形体,而Y不存在同素异形体 | |
| D. | X、M均能与氯形成由极性键构成的正四面体非极性分子 |
16.某化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中三次检验结果如下表所示,请回答下列问题.
(1)三次检验结果中第二次检验结果不正确.
(2)为了确定NH4+的存在,写出鉴定NH4+的实验方法和现象:取原溶液少许,加入浓NaOH溶液,微热,产生的气体能使湿润石蕊的红色石蕊试纸变蓝.
| 检验次数 | 溶液中检验出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NH4Cl |
| 第二次 | NH4Cl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、NH4Cl、K2CO3、NaCl |
(2)为了确定NH4+的存在,写出鉴定NH4+的实验方法和现象:取原溶液少许,加入浓NaOH溶液,微热,产生的气体能使湿润石蕊的红色石蕊试纸变蓝.
10.为达到下表所列的实验目的,所采用的实验方法正确的是( )
| 实验目的 | 实验方法 | |
| A | 检验某混合溶液中是否有Cl- | 取样滴加AgNO3溶液 |
| B | 检验氯化铵中的NH4+ | 加热后,用湿润的红色石蕊试纸靠近试管口 |
| C | 鉴别CO2和SO2 | 分别通入澄清石灰水 |
| D | 检验某试液中是否含有SO42- | 取样滴入盐酸酸化后,再滴入BaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |

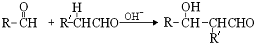
 .
. .
.
 .
.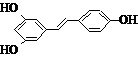 )属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用.某课题组提出了如下合成路线:
)属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用.某课题组提出了如下合成路线: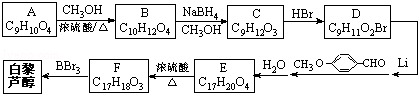

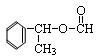
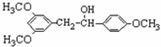 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$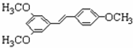 +H2O.
+H2O.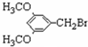 、E
、E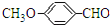 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式: .
. 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题: