题目内容
在一个定容密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A.0.1 mol·L-1·min-1 B.0.3 mol·L-1·min-1
C.0.2 mol·L-1·min-1 D.0.6 mol·L-1·min-1
C
【解析】
试题分析:氮气与氢气的反应方程式是N2(g)+3H2(g) 2NH3(g),10min后氮气的物质的量浓度减少1.8mol/L-0.8mol/L=1.0mol/L,则生成氨气的物质的量浓度是2×1.0mol/L=2.0mol/L,所以在这10min内NH3的平均反应速率是2.0mol/L/10min=0.2 mol·L-1·min-1,答案选C。
2NH3(g),10min后氮气的物质的量浓度减少1.8mol/L-0.8mol/L=1.0mol/L,则生成氨气的物质的量浓度是2×1.0mol/L=2.0mol/L,所以在这10min内NH3的平均反应速率是2.0mol/L/10min=0.2 mol·L-1·min-1,答案选C。
考点:考查反应速率的计算

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
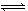 2NO+O2在恒温恒容密闭容器中反应,达到平衡状态的标志是
2NO+O2在恒温恒容密闭容器中反应,达到平衡状态的标志是
 CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是