题目内容
19.苯环结构中不存在碳碳单、双键交替出现的结构,下列可以作为证据的事实是( )①苯不能使高锰酸钾酸性溶液褪色 ②苯不能使溴水因发生化学反应而褪色
③苯在加热和有催化剂存在的条件下能生成环己烷 ④苯中碳碳键长完全相等
⑤邻二氯苯只有一种 ⑥间二氯苯只有一种.
| A. | ①②④⑤ | B. | ①②③④⑥ | C. | ①⑤ | D. | ①② |
分析 ①高锰酸钾溶液具有强氧化性,遇到含双键或三键等不饱和键的物质会褪色,苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键;
②苯若含有双键,则能够使溴水褪色;
③依据与氢气发生加成反应是不饱和键的性质;
④单键与双键键长不同;
⑤若是单双建交替,则邻二氯苯有2种;
⑥无论苯的结构中是否有碳碳双键和碳碳单键,苯的间位二元取代物都无同分异构体来分析.
解答 解:①苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在C-C单键与C=C双键的交替结构,故①正确;
②苯不能使溴水因发生化学反应而褪色,说明不含有碳碳双键,可以说明苯环结构中不存在碳碳单、双键交替出现的结构,故②正确;
③苯能在一定条件下跟H2加成生成环己烷,发生加成反应是双键或三键具有的性质,不能证明苯环结构中不存在C-C单键与C=C双键的交替结构,故③错误;
④苯中碳碳键长完全相等,说明苯环结构中不存在碳碳单、双键交替出现的结构,故④正确;
⑤若是单双建交替,则邻二氯苯有2种,而实际邻二氯苯只有一种说明苯环结构中不存在碳碳单、双键交替出现的结构,故⑤正确;
⑥无论苯的结构中是否有碳碳双键和碳碳单键,苯的间位二元取代物都无同分异构体,所以不能说明苯不是单双键交替结构,故⑥错误;
故选:A.
点评 本题考查苯的结构与性质,难度不大,综合性较大,要求知识掌握全面,能运用知识分析和解决问题,重在能力的考查.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
9.某海域海水一些化学成分如表所示,已知:25℃时,
Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11.
某化学小组同学欲在实验制备MgCl2,并提取Zn.设计流程如图:
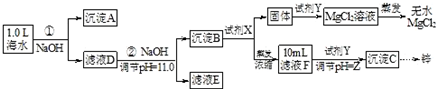
[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH> 7.0(填“>”、“<”、“﹦”),其原因是HCO3-+H2O?H2CO3+OH-(写离子方程式).
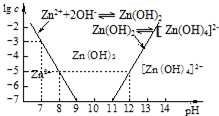
(2)如图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图.请结合图中数据回答:试剂Y的化学式为HCl;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH范围为8<pH<12.
(3)同学们发现,把MgCl2溶液蒸干、灼烧所得的白色固体难溶于水,你认为其主要成分是MgO.原因是(用化学方程式表示)MgCl2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2HCl↑、Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp=10-17.
Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11.
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |

[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH> 7.0(填“>”、“<”、“﹦”),其原因是HCO3-+H2O?H2CO3+OH-(写离子方程式).
(2)如图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图.请结合图中数据回答:试剂Y的化学式为HCl;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH范围为8<pH<12.

(3)同学们发现,把MgCl2溶液蒸干、灼烧所得的白色固体难溶于水,你认为其主要成分是MgO.原因是(用化学方程式表示)MgCl2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2HCl↑、Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp=10-17.
14.化合物G(结构如图)是合成抗癌药氨柔比星的中间体.下列说法正确的是( )
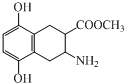

| A. | 该有机物的分子式为C12H14NO4 | |
| B. | 该有机物既可与盐酸反应,又可与NaOH溶液反应 | |
| C. | 该有机物中含有2个手性碳原子 | |
| D. | 1mol该有机物最多只能与1molBr2发生取代反应 |
4.乙烯与乙炔的混合气体完全燃烧时,消耗氧气的体积是混合气体的2.8倍,则原混合气体对氢气的相对密度为( )
| A. | 12.6 | B. | 13 | C. | 13.5 | D. | 13.6 |
18.下列说法正确的是( )
| A. | 随原子序数递增,ⅦA族元素的最高价氧化物对应水化物酸性逐渐增强 | |
| B. | 第三周期元素中(除稀有气体元素)简单离子半径最小的元素,其氧化物具有两性 | |
| C. | 第三周期气态氢化物的沸点均为同主族中沸点最低 | |
| D. | 第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |
19.硫元素的价电子较多,与氯能形成多种化合物.将Cl2通入熔融的硫磺可以制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊;而S2Cl2与NaOH 溶液反应可生成三种盐,得到澄清溶液.S2Cl2在合成橡胶,硬水软化等方面有着重要应用.有关S2Cl2的叙述正确的有( )
| A. | S2Cl2的结构简式:S-Cl-S-Cl | |
| B. | 13.5g S2Cl2和NaOH反应电子转移数为0.1NA | |
| C. | S2Cl2和NaOH水溶液反应,氧化与还原产物物质的量之比为1:1 | |
| D. | S2Cl2和水反应中,氧化剂还原剂物质的量之比为1:1 |

 ;
; ,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.
,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.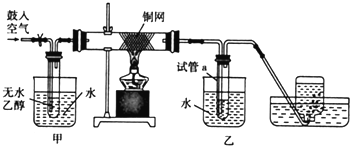
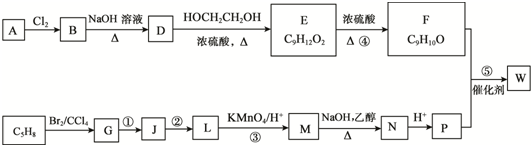
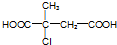 .
. (R1~R4表示烃基)
(R1~R4表示烃基) .
.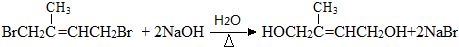 .
. .
. .
.