题目内容
20.下列物质属于电解质的是( )| A. | KMnO4 | B. | Cu | C. | 氨水 | D. | SO2 |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,电解质包括酸、碱、盐、金属氧化物和水等;在水溶液里或熔融状态下都不导电的化合物是非电解质,非电解质包括乙醇、蔗糖、非金属氧化物和氨气.
解答 解:A、高锰酸钾在水溶液中和熔融状态下均能电离出自由移动离子而导电,故为电解质,故A正确;
B、铜为单质,故既不是电解质也不是非电解质,故B错误;
C、氨水是氨气的水溶液,是混合物,既不是电解质也不是非电解质,故C错误;
D、二氧化硫在水溶液中和熔融状态下均不能导电,故为非电解质,故D错误.
故选A.
点评 本题考查了电解质的判断,难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.设NA为阿伏加德罗常数,则下列叙述不正确的是( )
| A. | 在标准状况下,22.4L的C6H14所含分子数为NA | |
| B. | 相同质量的H2和Cl2相比,H2的分子数多 | |
| C. | 2.3g金属Na变成Na+时失去的电子数目为0.1NA | |
| D. | 在1L0.1mol/L的HAc溶液中,所含Ac-与HAc之和为0.1NA |
8.下列离子方程式书写正确的是( )
| A. | 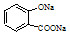 溶液通入少量CO2: 溶液通入少量CO2: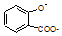 +CO2+H2O═ +CO2+H2O═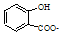 +HCO3- +HCO3- | |
| B. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3-可能会大量共存 | |
| C. | 少量SO2通入NaClO溶液中:SO2+ClO-+OH-=SO42-+Cl-+H+ | |
| D. | 5.6 g Fe与200 mL 2.0 mol/L HNO3溶液:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O |
5.下列有关实验操作设计、现象记录、结论解释都正确的是( )
| 选项 | 实验操作设计 | 现象记录 | 结论解释 |
| A | 将少量浓硝酸逐滴加入Cu和稀硫酸的混合物中 | 产生红棕色气体 | 硝酸被还原为NO2 |
| B | 用坩埚钳夹住铝箔在酒精灯上加热 | 铝箔熔化但并不滴落 | 熔点:Al2O3>Al |
| C | 向某氯化亚铁溶液中加入 Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化亚铁溶液已经变质 |
| D | 向AlCl3溶液中逐滴加入NaOH溶液至过量 | 产生大量的白色沉淀 | Al(OH)3难溶于水 |
| A. | A | B. | B | C. | C | D. | D |
12.某学生的实验报告所列出的下列数据中合理的是( )
| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用托盘天平称量25.20g NaCl | |
| D. | 用25mL碱式滴定管量取碱溶液21.70mL |
9.下列设计的实验方案能达到实验目的是( )
| A. | 制备银氨溶液:向2%的氨水中逐滴加入足量的2%的AgNO3溶液 | |
| B. | 除去MgCl2溶液中少量FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌,充分反应后过滤 | |
| C. | 比较Ag2CO3与AgCl溶度积大小:向浓度均为0.1mol•L-1的Na2CO3和NaCl的混合溶液中滴加0.1mol•L-1 AgNO3溶液,观察现象 | |
| D. | 验证Fe3+与I-的反应有一定限度:向5mL0.1mol•L-1KI溶液中滴入0.1mol•L-1FeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 |
18.水溶液中能大量共存的一组离子是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+ H+ SO42- HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、NH4+、NO3-、OH- |