题目内容
已知某反应的焓变小于零,则下列叙述正确的是( )
| A、该反应一定是放热反应 |
| B、该反应一定是吸热反应 |
| C、该反应中反应物的总能量一定小于产物的总能量 |
| D、该反应需要加热才能发生 |
考点:焓变和熵变
专题:化学反应中的能量变化
分析:△H=生成物总能量-反应物总能量,某反应的焓变小于零,说明正反应放热,反应物总能量高于生成物,据此分析.
解答:
解:△H=生成物总能量-反应物总能量,某反应的焓变小于零,说明正反应放热,反应物总能量高于生成物,
A、该反应一定是放热反应,故A正确;
B、该反应一定是放热反应,故B错误;
C、反应物总能量高于生成物,故C错误;
D、正反应放热有的需要加热,有的不需要加热,故D错误;
故选A.
A、该反应一定是放热反应,故A正确;
B、该反应一定是放热反应,故B错误;
C、反应物总能量高于生成物,故C错误;
D、正反应放热有的需要加热,有的不需要加热,故D错误;
故选A.
点评:本题考查了放热反应反应物总能量高于生成物的判断,题目难度不大,注意把握△H=生成物总能量-反应物总能量;

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子能大量共存的是( )
| A、A、H+、Na+、Si032-、Cl- |
| B、Al3+、Fe3+、SO42-、SCN- |
| C、Mg2+、Na+、NO3-、SO42- |
| D、H+、K+、NO3-、AlO2- |
有关原电池的下列说法中正确的是( )
| A、在外电路中电子由正极流向负极 |
| B、在原电池中,只有金属锌作为负极 |
| C、原电池工作时,阳离子向正极方向移动 |
| D、原电池工作时,阳离子向负极方向移动 |
下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
A、2NaCl(s)+H2SO4(浓)
| ||||
B、C+2H2SO4(浓)
| ||||
C、Cu+2H2SO4(浓)
| ||||
D、2FeO+4H2SO4(浓)
|
在25℃时,将两个铂电极插入到一定量的Na2SO4饱和溶液中电解,通电一段时间后,在阴极逸出a mol气体,同时有Wg Na2SO4.10H2O晶体析出.若温度不变,此时剩余Na2SO4溶液的质量分数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
标准状况下2.24LCO气体在足量氧气中燃烧后,加足量的过氧化钠充分吸收气体后,过氧化钠质量增加了( )
| A、2.8g | B、4.4g |
| C、10.6g | D、1.4g |
下列离子方程式正确的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ | ||||
| B、NO2与水的反应:3NO2+H2O=2NO3-+2H++NO | ||||
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ | ||||
D、用铂电极电解氯化镁溶液:2Cl-+2H2O
|
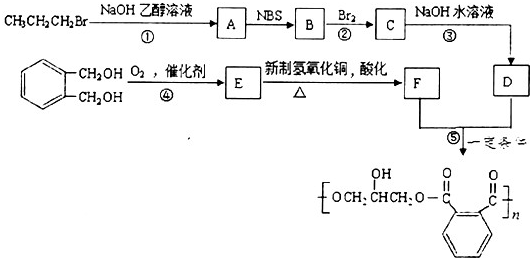
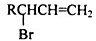
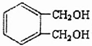 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有