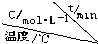题目内容
下列关于电解池的叙述不正确的是( )
| A、在电解池的阴极发生还原反应 |
| B、与电源负极相连的是电解池的阳极 |
| C、阴离子移向电解池的阳极 |
| D、电子从电源的负极沿导线流入电解池的阴极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电解池中,与外接电源负极相连的为阴极,阴极得电子发生还原反应,与正极相连的为阳极,阳极上失电子发生氧化反应,电子从负极经导线流入阴极,电解池内,阴离子移向电解池的阳极,阳离子移向电解池的阴极,据此分析.
解答:
解:A、电解池中,与外接电源负极相连的为阴极,阳离子在阴极得电子发生还原反应,故A正确;
B、电解池中,与外接电源负极相连的为阴极,故B错误;
C、阴离子移向电解池的阳极,阳离子移向电解池的阴极,故C正确;
D、电子从负极经导线流入阴极,阳离子在阴极得电子,故D正确;
故选B.
B、电解池中,与外接电源负极相连的为阴极,故B错误;
C、阴离子移向电解池的阳极,阳离子移向电解池的阴极,故C正确;
D、电子从负极经导线流入阴极,阳离子在阴极得电子,故D正确;
故选B.
点评:本题考查电解池知识,侧重于考查学生的化学知识的综合运用,难度不大,注意把握电解池的工作原理.

练习册系列答案
相关题目
在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),达到平衡时,生成了2mol C,经测定D的浓度为0.5mol?L-1,下列判断正确的是( )
| A、X=3 |
| B、A的转化率为50% |
| C、平衡时B的浓度为1.5 mol?L-1 |
| D、达到平衡时,在相同温度下容器内混合气体的压强是反应前的95% |
可逆反应mA(g)?nB(g)+pC(s)△H=QKJ/moL,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( )


| A、m>n,Q>0 |
| B、m<n+p,Q>0 |
| C、m>n,Q<0 |
| D、m>n+p,Q<0 |
下列关于氯水的叙述,正确的是( )
| A、氯水中只含Cl2和H2O两种分子 |
| B、新制氯水只能使蓝色石蕊试纸变红 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后其pH将变小,酸性增强 |
下列事实:
①NaHCO3溶液呈碱性
②NaHSO4溶液呈酸性
③长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结
④加热能增加纯碱的去污能力
⑤配制CuCl2溶液,用稀盐酸溶解CuCl2固体
⑥明矾能净水
⑦氯化铵溶液可作焊药去除金属制品表面的锈斑
⑧加热FeCl3?6H2O晶体,往往得不到FeCl3固体
⑨NH4F溶液不能用玻璃瓶盛放.其中与盐类水解知识有关的是( )
①NaHCO3溶液呈碱性
②NaHSO4溶液呈酸性
③长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结
④加热能增加纯碱的去污能力
⑤配制CuCl2溶液,用稀盐酸溶解CuCl2固体
⑥明矾能净水
⑦氯化铵溶液可作焊药去除金属制品表面的锈斑
⑧加热FeCl3?6H2O晶体,往往得不到FeCl3固体
⑨NH4F溶液不能用玻璃瓶盛放.其中与盐类水解知识有关的是( )
| A、全部 | B、除②⑦以外 |
| C、除②以外 | D、除⑨以外 |
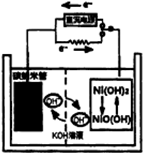 一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )
一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )| A、储存H2的碳纳米管放电时为负极,充电时为阳极 |
| B、充电时阳极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
| C、放电时正极附近溶液的pH减小 |
| D、放电时负极反应为H2+2OH--2e-=2H2O |
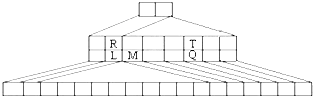 如图是另一种元素周期表--三角形元素周期表的一部分,图中标示了L、M、Q、R、T元素的位置,下列判断正确的是:( )
如图是另一种元素周期表--三角形元素周期表的一部分,图中标示了L、M、Q、R、T元素的位置,下列判断正确的是:( )| A、Q、T两元素的氢化物的稳定性为HnT<HnQ |
| B、L、R的单质与盐酸反应速率为R>L |
| C、M与T形成的化合物有两性 |
| D、L、Q形成的简单离子核外电子数相等 |
物质发生化学变化时,下列量在反应前后肯定不发生变化的是( )
①电子总数 ②原子总数 ③分子总数 ④物质的种类 ⑤物质的总质量 ⑥质子总数.
①电子总数 ②原子总数 ③分子总数 ④物质的种类 ⑤物质的总质量 ⑥质子总数.
| A、①②③⑤ | B、①②⑤⑥ |
| C、②③⑤⑥ | D、①④⑤ |
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法: