��Ŀ����
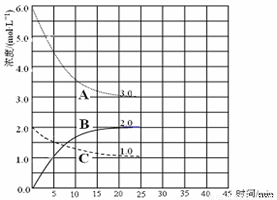
��һ���¶��£���1 mol��N2O4���ܱ������У�����ѹǿ���䣮�����¶���T1�Ĺ����У���������ɫ��Ϊ����ɫ���¶���T1������T2�Ĺ����У���������Ϊ��ɫ��������T2���䣬����ѹǿ��������Ϊ����ɫ����������ʵ���(n)���¶�(T)�仯�Ĺ�ϵ��ͼ��

(1)�����¶���T1�Ĺ����У���������ɫ��Ϊ����ɫ�Ļ�ѧ����ʽ________��
(2)T1��T2֮�䣬��Ӧ�Ļ�ѧ����ʽ________��
(3)T2��T3֮�䣬�����ƽ��Ħ��������________��
�𰸣�
������
������
|
����(1)N2O4 ����(2)2NO2 ����(3)30.67 g/mol(ȱ��λ��1��) |

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ

 2NH3(g)+
2NH3(g)+ O2(g) ��H="+765.0kJ" /mol��
O2(g) ��H="+765.0kJ" /mol��