题目内容
下列物质的电子式,正确的是( )
A、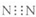 | B、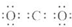 | C、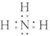 | D、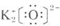 |
分析:A.氮气分子中每个氮原子含有一个孤电子对;
B.二氧化碳分子中每个氧原子和碳原子形成两个共用电子对,每个氧原子含有2个孤电子对;
C.氨气分子中每个氢原子和氮原子形成一个共用电子对;
D.氧化钾电子式的书写中钾离子不能合并.
B.二氧化碳分子中每个氧原子和碳原子形成两个共用电子对,每个氧原子含有2个孤电子对;
C.氨气分子中每个氢原子和氮原子形成一个共用电子对;
D.氧化钾电子式的书写中钾离子不能合并.
解答:解:A.氮气分子中每个氮原子含有一个孤电子对,氮气分子的电子式为 ,故A错误;
,故A错误;
B.二氧化碳分子中每个氧原子和碳原子形成两个共用电子对,每个氧原子含有2个孤电子对,二氧化碳分子的电子式为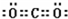 ,故B错误;
,故B错误;
C.氨气分子中每个氢原子和氮原子形成一个共用电子对,所以氨气分子的电子式为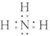 ,故C正确;
,故C正确;
D.氧化钾电子式的书写中钾离子不能合并,氧化钾的电子式为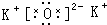 ,故D错误;
,故D错误;
故选C.
 ,故A错误;
,故A错误;B.二氧化碳分子中每个氧原子和碳原子形成两个共用电子对,每个氧原子含有2个孤电子对,二氧化碳分子的电子式为
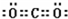 ,故B错误;
,故B错误;C.氨气分子中每个氢原子和氮原子形成一个共用电子对,所以氨气分子的电子式为
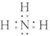 ,故C正确;
,故C正确;D.氧化钾电子式的书写中钾离子不能合并,氧化钾的电子式为
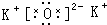 ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式的书写,明确电子式的书写规则是解本题关键,注意离子化合物和共价化合物电子式的书写区别,易错选项是A,注意部分物质的电子式易漏掉孤电子对而导致错误,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
(13分)⑴完成下列物质的电子式:
KOH ; H2S ;
CS2 ; NH4Cl ;
⑵下列微粒之间,属于同位素的是 ,(填序号,下同)属于同素异形体的是 ,属于同分异构体的是 ,固体时属于原子晶体的是 。
| A.正丁烷与异丁烷 |
| B.红磷与白磷 |
| C.氕与氚 |
| D.氯化钠与干冰 |
F.氧气和臭氧
G. 13C和14C
H.CH3OCH3和CH3CH2OH
⑶亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
Na2SO3+ KIO3+ H2SO4—— Na2SO4+ K2SO4+ I2+ H2O
(a)配平上面的氧化还原反应方程式,将系数填入方框中。
(b)其中氧化剂是 ,若反应中有5 mol电子转移,则生成的碘是 mol。