题目内容
19.某固体粉末样品中只可能含有Fe2+、Fe3+、Na+、NH4+、Cl-中的几种离子,某实验小组为确定其成分设计如下实验:①取适量样品加水溶解.
②取少量①中的待测液,滴加KSCN溶液,无明显现象,再滴加少量氯水,溶液变为血红色.
③另取少量①中的待测液,滴加过量的氢氧化钠溶液,除得到沉淀外,还有无色有刺激性气味的气体放出,该气体可使酚酞溶液变红.
(1)由上述实验可知,该样品中一定不含有的离子为Fe3+(填离子符号),一定含有的离子为Fe2+、NH4+、Cl-(填离子符号).
(2)操作③中沉淀变化的现象为沉淀由白色迅速变为灰绿色,最终变为红褐色.
(3)操作③中生成刺激性气体的离子方程式为NH4++OH-=NH3↑+H2O.
分析 ①取适量样品加水溶解.
②取少量①中的待测液,滴加KSCN溶液,无明显现象,再滴加少量氯水,溶液变为血红色,说明溶液中含有Fe2+,不含Fe3+;
③另取少量①中的待测液,滴加过量的氢氧化钠溶液,除得到沉淀外,还有无色有刺激性气味的气体放出,该气体可使酚酞溶液变红,则含有NH4+,由溶液的电中性原则可知一定含有Cl-,以此解答该题.
解答 解:(1)由以上分析可知一定不含Fe3+,一定含有Fe2+、NH4+、Cl-,故答案为:Fe3+;Fe2+、NH4+、Cl-;
(2)含有亚铁离子,加入氢氧化钠溶液,生成白色氢氧化亚铁沉淀,氢氧化亚铁不稳定,可被氧化生成氢氧化铁,现象是沉淀由白色迅速变为灰绿色,最终变为红褐色,故答案为:沉淀由白色迅速变为灰绿色,最终变为红褐色;
(3)生成的刺激性气味的气体为氨气,反应的离子方程式为NH4++OH-=NH3↑+H2O,故答案为:NH4++OH-=NH3↑+H2O.
点评 本题考查无机物的推断,为高频考点,把握常见离子之间的反应、反应现象推断物质为解答的关键,侧重分析、实验、推断及计算能力的综合考查,题目难度中等.

练习册系列答案
相关题目
9.下列四组离子中一定能大量共存的是( )
| A. | K+、H+、Cl-、CO32- | B. | Fe3+、Mg2+、NO3-、SCN- | ||
| C. | NO3- H+、Fe2+、SO42- | D. | Na+、OH-、Cl-、NO3- |
10.表是元素周期表的一部分,根据所给的10种元素,完成以下各小题..
(1)镁的原子结构示意图为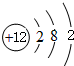 .
.
(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al (OH)3中,属于两性氢氧化物的是Al(OH)3.它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为Al(OH)3+3H+═Al3++3H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
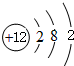 .
.(2)H2SO4与HClO4中,酸性较强的是HClO4.
(3)NaOH与Al (OH)3中,属于两性氢氧化物的是Al(OH)3.它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为Al(OH)3+3H+═Al3++3H2O.
4.化学与生活、生产、环境密切相关,下列有关说法错误的是( )
| A. | K2FeO4和明矾都可做水处理剂,但工作原理不完全相同 | |
| B. | 氢能是一种新型能源,具有热值高、资源丰富、无毒、无污染的优点 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 合成氨工业中,使用催化剂不能提高H2和N2的转化率 |
11.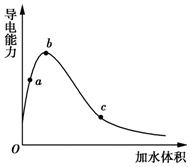 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )| A. | a、b、c三点溶液的pH:c<a<b | |
| B. | 用湿润的pH试纸测量a处溶液的pH,测量结果偏小 | |
| C. | a、b、c三点CH3COOH的电离程度:c<a<b | |
| D. | a、b、c三点溶液用1 mol•L-1 NaOH溶液中和,消耗NaOH溶液体积:c<a<b |
8.已知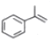 (异丙烯苯)$→_{一定条件}^{+H_{2}}$
(异丙烯苯)$→_{一定条件}^{+H_{2}}$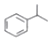 (异丙苯),下列说法错误的是( )
(异丙苯),下列说法错误的是( )
 (异丙烯苯)$→_{一定条件}^{+H_{2}}$
(异丙烯苯)$→_{一定条件}^{+H_{2}}$ (异丙苯),下列说法错误的是( )
(异丙苯),下列说法错误的是( )| A. | 反应属于加成反应 | B. | 异丙苯的一氯代物共有6种 | ||
| C. | 可用溴水鉴别异丙烯苯和异丙苯 | D. | 异丙苯是苯的同系物 |
9.下列关于有机化合物的说法正确的是( )
| A. | 1-丁醇的结构简式可写作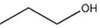 | |
| B. | 氨基酸合成多肽链属于加聚反应 | |
| C. | 分子式为C4H8O2,既含有羟基又含有醛基的同分异构体有5种 | |
| D. | 糖、油脂、蛋白质等这些人体必需的营养物质都是高分子化合物 |