题目内容
14.镍有电镀和化学镀两种方法,化学镀反应原理:Ni2++H2PO2-+H2O═Ni+H2PO3-+2H+.下列说法错误的是( )| A. | 电镀镍时,Ni为阴极,镀件为阳极 | |
| B. | 电镀和化学镀原理都是利用氧化还原反应 | |
| C. | 化学镀无需通电,对镀件的导电性无特殊要求 | |
| D. | 化学镀中H2PO2-中P化合价为+1,有强还原性 |
分析 A、电镀镍时,镀件为阴极,镀层金属为阳极;
B、电镀和化学镀原理都是金属析出的反应;
C、化学镀是在金属表面析出金属单质的过程,不是电解原理;
D、根据化合价规则确定元素的化合价,判断物质的性质.
解答 解:A、电镀镍时,镀件为阴极,镀层金属Ni为阳极,故A错误;
B、电镀和化学镀原理都是金属析出的反应,都是利用氧化还原反应,故B正确;
C、化学镀是在金属表面析出金属单质的过程,不是电解原理,化学镀无需通电,对镀件的导电性无特殊要求,故C正确;
D、根据化合价规则,H是+1价,O是-2价,H2PO2-中P化合价为+1,有强还原性,故D正确.
故选A.
点评 本题考查学生电镀以及化学镀的原理知识,注意知识的区别和联系,知识的迁移应用是关键,难度中等.

练习册系列答案
相关题目
4.一定质量的混合气体在密闭容器中发生如下反应:xA(气)+yB(气)?zC(气).达到平衡后,测得A气体的浓度为0.5mol/L.当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L.下列叙述正确的是( )
| A. | 平衡向正反应方向移动 | B. | x+y>z | ||
| C. | C的体积分数增大 | D. | B的转化率增大 |
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 500 mL1 mol/L MgCl2溶液中含有Cl-数目为0.5NA | |
| B. | 标准状况下,33.6L SO3与48gO2所占的体积相等 | |
| C. | 17 gNH3含有的电子个数为l0NA | |
| D. | 1 mol O2与2 mol SO2一定条件下混合反应,可生成2 mol SO3 |
9.AgN03是一种重要的化学试剂,精炼铜的阳极泥中含有较多的银,可用于制备AgN03,主要工艺流程如图:

已知:AgNO3与Cu( N03)2受热易分解,分解温度如表所示.
(1)黑色固体D的化学式为CuO,①中加热温度的范围应控制在473-673K.
(2)如表为不同温度时AgNO3的溶解度
据此判断,②中从溶液Ⅱ中获得纯净的AgN03晶体的主要操作为:蒸发浓缩→过滤冷却结晶→过滤→洗涤→干燥.
(3)气体甲可以与NaOH溶液反应,产物之一为NaN02.已知常温时Ka(HN02)=4.9x10-4,常温下将0.1mol•L-1 NaOH溶液与0.2mol•L-1HN02溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
(4)另一种提纯AgN03溶液的方法为:向含有Cu2+的AgNO3溶液中加入某固体,充分反应后滤去蓝色沉淀即可,该固体可以为D(填选项字母).
A.NaOH B.AgCl C.FeS D.Ag2O
(5)制得的AgN03可配制为标准溶液,在中性或弱碱性溶液中,以K2Cr04为指示剂测定氯化物中Cl-的含量,主要反应为:
Ag++Cl-═AgCl↓ 2Ag++Cr042-(黄色)═Ag2Cr04↓砖红色)
已知Ksp(AgCl)=1.8×lO-10,Ksp(AgCrO4)=1.2×l0-12,则用该方法测定NaCl溶液中的c(Cl-)时,达到滴定终点时的现象为当滴入最后一滴AgNO3后有砖红色沉淀生成;实验中指示剂K2Cr04的浓度不宜过大,原因为K2CrO4溶液为黄色,浓度过大将影响滴定终点现象的判断(或K2CrO4溶液浓度过大时,有可能会在Cl-未完全沉淀时与Ag+结合,对滴定结果造成误差).

已知:AgNO3与Cu( N03)2受热易分解,分解温度如表所示.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 122 | 216 | 311 | 440 | 585 | 733 |
(2)如表为不同温度时AgNO3的溶解度
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 122 | 216 | 311 | 440 | 585 | 733 |
(3)气体甲可以与NaOH溶液反应,产物之一为NaN02.已知常温时Ka(HN02)=4.9x10-4,常温下将0.1mol•L-1 NaOH溶液与0.2mol•L-1HN02溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
(4)另一种提纯AgN03溶液的方法为:向含有Cu2+的AgNO3溶液中加入某固体,充分反应后滤去蓝色沉淀即可,该固体可以为D(填选项字母).
A.NaOH B.AgCl C.FeS D.Ag2O
(5)制得的AgN03可配制为标准溶液,在中性或弱碱性溶液中,以K2Cr04为指示剂测定氯化物中Cl-的含量,主要反应为:
Ag++Cl-═AgCl↓ 2Ag++Cr042-(黄色)═Ag2Cr04↓砖红色)
已知Ksp(AgCl)=1.8×lO-10,Ksp(AgCrO4)=1.2×l0-12,则用该方法测定NaCl溶液中的c(Cl-)时,达到滴定终点时的现象为当滴入最后一滴AgNO3后有砖红色沉淀生成;实验中指示剂K2Cr04的浓度不宜过大,原因为K2CrO4溶液为黄色,浓度过大将影响滴定终点现象的判断(或K2CrO4溶液浓度过大时,有可能会在Cl-未完全沉淀时与Ag+结合,对滴定结果造成误差).
19.鉴别Na2CO3与NaHCO3两种溶液,可以用下列试剂中的( )
| A. | 盐酸 | B. | NaOH溶液 | C. | Ca(OH)2溶液 | D. | CaCl2溶液 |
6.元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,下列判断正确的是( )
| R | ||
| X | T | Z |
| Q |
| A. | X的最高价氧化物能溶于强碱 | B. | 非金属性:T>R | ||
| C. | 单质导电性:Z>T>X | D. | R与Q的原子核外电子数相差16 |
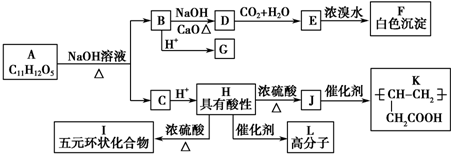
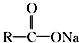 +NaOH$→_{△}^{CaO}$R═H+Na2CO3
+NaOH$→_{△}^{CaO}$R═H+Na2CO3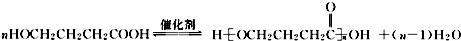 .
. .
.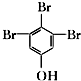 (写结构简式).
(写结构简式).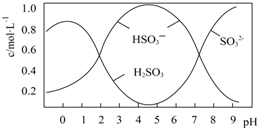 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.