题目内容
已知氧化钠和过氧化钠均能和二氧化碳反应,但氧化钠与二氧化碳反应不生成氧气,现有一定量的氧化钠和过氧化钠的混合物,使其充分与二氧化碳反应,每吸收17.60g二氧化碳,就有3.2g氧气放出,试计算混合物中氧化钠和过氧化钠的质量分数.
考点:有关混合物反应的计算
专题:
分析:根据n=
计算出二氧化碳、氧气的物质的量,再根据反应方程式2Na2O2+2CO2=2Na2CO3+O2计算出过氧化钠的物质的量,然后根据二氧化碳的物质的量计算出消耗氧化钠的物质的量,然后分别计算出混合物中氧化钠、过氧化钠的质量分数.
| m |
| M |
解答:
解:17.6g二氧化碳的物质的量为:
=0.4mol,
3.2g氧气的物质的量为:
=0.1mol,
由于二氧化碳足量,氧化钠和过氧化钠完全反应,
根据反应2Na2O2+2CO2=2Na2CO3+O2可知,该混合物中含有过氧化钠的物质的量为:0.1mol×2=0.2mol,过氧化钠完全反应消耗了0.2mol二氧化碳,0.2mol过氧化钠的质量为:78g/mol×0.2mol=15.6g,
根据反应可知Na2O+CO2=Na2CO3,该混合物中含有氧化钠的物质的量为0.2mol,质量为:62g/mol×0.2mol=12.4g,
混合物的总质量为:15.6g+12.4g=28g,
混合物中氧化钠的质量分数为:
×100%=44.3%,过氧化钠的质量分数为:
×100%=55.7%,
答:混合物中氧化钠的质量分数为44.3%,过氧化钠的质量分数为55.7%.
| 17.6g |
| 44g/mol |
3.2g氧气的物质的量为:
| 3.2g |
| 32g/mol |
由于二氧化碳足量,氧化钠和过氧化钠完全反应,
根据反应2Na2O2+2CO2=2Na2CO3+O2可知,该混合物中含有过氧化钠的物质的量为:0.1mol×2=0.2mol,过氧化钠完全反应消耗了0.2mol二氧化碳,0.2mol过氧化钠的质量为:78g/mol×0.2mol=15.6g,
根据反应可知Na2O+CO2=Na2CO3,该混合物中含有氧化钠的物质的量为0.2mol,质量为:62g/mol×0.2mol=12.4g,
混合物的总质量为:15.6g+12.4g=28g,
混合物中氧化钠的质量分数为:
| 12.4g |
| 28g |
| 15.6g |
| 28g |
答:混合物中氧化钠的质量分数为44.3%,过氧化钠的质量分数为55.7%.
点评:本题考查了混合物反应的计算,题目难度中等,明确氧化钠、过氧化钠的与二氧化碳的反应原理为解答关键,注意明确质量分数的概念及计算方法.

练习册系列答案
相关题目
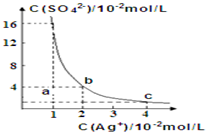 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是( )| A、含有大量SO42-的溶液中肯定不存在Ag+ |
| B、Ag2SO4的溶度积常数(Ksp)为8×10-4 |
| C、a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
| D、0.02mol?L-1的AgNO3溶液与0.2mol?L-1的Na2SO4溶液等体积混合不会生成沉淀 |


