题目内容
25℃时,用0.1mol/L的醋酸溶液做了以下实验,不能证明其为弱酸的是( )
| A、pH大于1 |
| B、溶液中含有HAc分子 |
| C、溶液中含有OH- |
| D、导电能力比0.1mol/L的盐酸弱 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:要证明醋酸为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答:
解:A、pH大于1,说明醋酸中氢离子浓度小于0.1mol/L,则能证明其为弱酸,故A错误;
B、溶液中含有HAc分子,说明醋酸不完全电离,属于弱酸,故B错误;
C、任何溶液中均会含有氢氧根离子,不能说明醋酸是弱酸,故C正确;
D、0.1mol/L的醋酸溶液导电能力比0.1mol/L的盐酸弱,说明醋酸中离子浓度小于盐酸中的离子浓度,盐酸是强酸,醋酸是弱酸,故D错误.
故选C.
B、溶液中含有HAc分子,说明醋酸不完全电离,属于弱酸,故B错误;
C、任何溶液中均会含有氢氧根离子,不能说明醋酸是弱酸,故C正确;
D、0.1mol/L的醋酸溶液导电能力比0.1mol/L的盐酸弱,说明醋酸中离子浓度小于盐酸中的离子浓度,盐酸是强酸,醋酸是弱酸,故D错误.
故选C.
点评:本题考查实验方案的评价,侧重于弱酸的实验角度的探究,注意把握实验原理和角度,学习中注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、澄清的石灰水与盐酸反应:Ca(OH)2+2H+=Ca2++2H2O | ||||
| B、钠与水的反应:Na+2H2O=Na++2OH-+H2↑ | ||||
C、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO
| ||||
| D、大理石溶于醋酸的反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
某学生使用托盘天平称食盐时,错误的将食盐放在右托盘,而把砝码放在左托盘,称得食盐的质量为15.5g(1g以下只能使用游码).如果按正确的放法,食盐的质量应为( )
| A、15.5g |
| B、15.0g |
| C、14.5g |
| D、14.0g |
除去苯中所含的苯酚,可采用的适宜方法是( )
| A、加足量NaOH溶液,分液 |
| B、加适量 浓溴水,过滤 |
| C、加70℃以上的热水,分液 |
| D、加适量FeCl3溶液,过滤 |
北京时间10月10日,两位美国科学家罗伯特?莱夫科维茨和布莱恩?克比尔卡因“G蛋白偶联受体研究”获得2012年诺贝尔化学奖.经研究发现,大约一半的药物是通过G蛋白偶联受体起作用的.下列说法正确的是( )
| A、人体必需的蛋白质都可通过体内合成 |
| B、重金属能使蛋白质变性 |
| C、多肽是构成蛋白质的最基本单元 |
| D、含有三个肽键的多肽称为三肽 |
下列电离方程式中,正确的是( )
| A、CH3COOH=CH3COO-+H+ |
| B、KClO3?K++ClO3- |
| C、NaOH=Na++OH- |
| D、NaHSO4=Na++HSO4- |
A和B两种有机物可以互溶,其有关性质如下表所示:
要除去A和B的混合物中的少量A得到B可采用的方法是( )
| 密度(20?C) | 熔点 | 沸点 | 熔解性 | |
| A | 0.713 7g?cm?3 | -116.3?C | 34.5?C | 不溶于水 |
| B | 0.789 3g?cm?3 | -117.3?C | 78.5?C | 与水以任意比混溶 |
| A、蒸馏 | B、重结晶 |
| C、萃取 | D、加水充分振荡,分液 |
对符号中“3”所表示的含义,说法不正确的是( )
| A、3O2--表示三个氧分子 | ||
| B、SO3--表示一个三氧化硫分子中含有三个氧元素 | ||
C、
| ||
| D、3H--表示三个氢原子 |
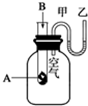 为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题: