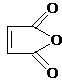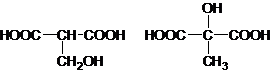题目内容
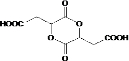
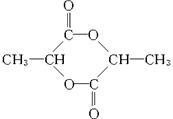
下列有关物质结构和元素周期律的表述正确的是( )
分析:A.同周期从左向右元素的非金属性增强;
B.第二周期ⅣA族元素的为C元素,则原子核电荷数一定为6,但中子数不一定为6;
C.主族元素中F、O没有正价;
D.氨气溶于水,溶于显碱性.
B.第二周期ⅣA族元素的为C元素,则原子核电荷数一定为6,但中子数不一定为6;
C.主族元素中F、O没有正价;
D.氨气溶于水,溶于显碱性.
解答:解:A.因同周期从左向右元素的非金属性增强,则ⅦA族元素是同周期中非金属性最强的元素,故A正确;
B.第二周期ⅣA族元素的为C元素,则原子核电荷数一定为6,但中子数不一定为6,如13C的中子数为7,故B错误;
C.一般主族元素的最高正价均等于其族序数,但主族元素中F、O没有正价,则O、F除外,故C错误;
D.绝大多数非金属元素的气态氢化物溶于水后,水溶液为酸性,但氨气溶于水,溶于显碱性,故D错误;
故选A.
B.第二周期ⅣA族元素的为C元素,则原子核电荷数一定为6,但中子数不一定为6,如13C的中子数为7,故B错误;
C.一般主族元素的最高正价均等于其族序数,但主族元素中F、O没有正价,则O、F除外,故C错误;
D.绝大多数非金属元素的气态氢化物溶于水后,水溶液为酸性,但氨气溶于水,溶于显碱性,故D错误;
故选A.
点评:本题考查元素周期律,题目难度中等,熟悉元素周期律即可解答,但应注意利用特例来分析解答.

练习册系列答案
相关题目