题目内容
20.X、Y、Z、D、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX,ZX焰色反应为黄色;Y、D同主族,可形成DY2、DY3两种分子.请回答下列问题:(1)D在元素周期表中的位置为第三周期ⅥA族.Y、Z、D的原子半径由大到小的顺序为Na>S>O(用元素符号表示).
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是HClO4(写化学式),非金属气态氢化物中还原性最强的是H2S(写化学式).
(3)由Y、G两元素形成的可作饮用水消毒剂的化合物的是ClO2(写化学式).
分析 X、Y、Z、D、G五种元素分属三个短周期,且原子序数依次增大,X、Z同主族,可形成离子化合物ZX,ZX焰色反应为黄色,可推知X为H,Z为Na;根据Y、D同主族,可形成DY2、DY3两种分子,可推知D为S,Y为O,则G只能是Cl.
解答 解:X、Y、Z、D、G五种元素分属三个短周期,且原子序数依次增大,X、Z同主族,可形成离子化合物ZX,ZX焰色反应为黄色,可推知X为H,Z为Na;根据Y、D同主族,可形成DY2、DY3两种分子,可推知D为S,Y为O,则G只能是Cl.
(1)D为S元素,在元素周期表中的位置为:第三周期ⅥA族,同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>S>O,故答案为:第三周期ⅥA族;Na>S>O;
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是HClO4,上述元素中S元素非金属性最弱,非金属气态氢化物中还原性最强的是:H2S,故答案为:HClO4;H2S;
(3)由O、Cl两元素形成的可作饮用水消毒剂的化合物的是:ClO2,故答案为:ClO2.
点评 本题考查结构性质位置关系应用,比较基础,注意对元素周期律的理解与应用,有利于基础知识的巩固.

练习册系列答案
相关题目
11.下列事实可用勒夏特列原理解释的是( )
| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 硫酸工业中,将黄铁矿粉碎后加入沸腾炉中 | |
| C. | 500℃左右比在室温时更有利于提高合成氨的转化率 | |
| D. | 对2HI?H2+I2平衡体系增加压强使颜色变深 |
8.下列离子方程式中,正确的是( )
| A. | 氨气通入醋酸中:CH3COOH+NH3═CH3COO-+NH4+ | |
| B. | 向碳酸氢镁溶液中加过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| C. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| D. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
15.一定量的某有机物和足量的钠反应,可得到气体VA L,等质量的该有机物与足量的纯碱溶液反应,可得到气体VB L.若同温、同压下VA>VB,则该有机物可能是( )
| A. | HO(CH2)2CHO | B. | HO(CH2)2COOH | C. | HOOC-COOH | D. | CH3COOH |
5.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )
| A. | 煤炭经过干馏,石油经分馏、裂化、裂解化工处理,可获得清洁能源和重要的化工原料 | |
| B. | 比能量低而笨重的铅蓄电池使用时电压不稳定,所以有被其他新型电池取代的趋势 | |
| C. | 玛瑙饰品的主要成分与建筑材料砂子相同 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制备电脑芯片 |
12.一种熔融碳酸盐燃料电池工作原理如图所示.则下列推断错误的是( )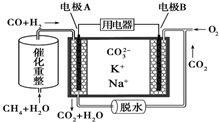

| A. | 放电时负极有CO2生成 | |
| B. | 正极反应为O2+2CO2+4e-═2CO32- | |
| C. | 反应CH4+H2O$→_{△}^{催化剂}$3H2+CO,每消耗1molCH4转移6mol 电子 | |
| D. | 该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
9.电石制取乙炔产生大量废渣:电石渣(主要成分为Ca(OH)2,另外还含有Fe和Al化学物及SO2等杂质),可用下面工艺实现电石渣吸收氯碱工业废气中的氯气,综合治理废渣和废气,回答下列问题:
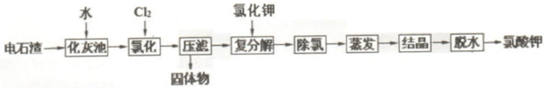
已知:①几种物质溶解度与温度的关系
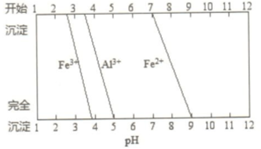
②几种离子开始和完全沉淀与pH的关系图
(1)某导电塑料是以乙炔为单体加聚合成,其化学为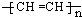 .
.
(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.

已知:①几种物质溶解度与温度的关系
| 温度/ | 0 | 10 | 20 | 30 | 40 |
| S(CaCl2)/g | 59.5 | 64.7 | 74.5 | 100 | 128 |
| S[Ca(ClO3)2]/g | 209 | ||||
| S(KClO3)/g | 3.3 | 5.2 | 7.3 | 10.2 | 13.9 |

(1)某导电塑料是以乙炔为单体加聚合成,其化学为
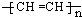 .
.(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.
1.下列说法正确的是( )
| A. | 体系有自发地向混乱度增加(即熵增)的方向转变的倾向,这是自然界的普遍规律 | |
| B. | 判断过程的自发性能确定过程能否发生和过程发生的速率 | |
| C. | 其它条件相同时,增大反应物浓度能使分子获得能量,活化分子百分数提高,反应速率增大 | |
| D. | 催化剂不影响反应活化能,从而只影响反应速率,不影响化学平衡 |