题目内容
16.实验室需要配制95mL1mol/L NaOH溶液,请回答下列问题:(1)实验仪器:托盘天平、小烧杯、钥匙、胶头滴管、玻璃棒、量筒、试剂瓶和100mL容量瓶.
(2)实验步骤:①计算;②称量;③溶解;④移液;⑤洗涤;⑥定容;⑦摇匀;⑧装瓶.在用托盘天平称量时,需要准确称量NaOH固体4.0g;将蒸馏水注入容量瓶,至液面距容量瓶颈刻度线下1-2cm时,改用胶头滴管滴加蒸馏水至刻度线.
(3)误差分析:下列实验操作中,可能导致溶液浓度偏高的是A E(填字母)
A.固体氢氧化钠溶解时未冷却至室温,就开始转移、洗涤以及定容;
B.转移时不小心有少量溶液流到了容量瓶外;
C.定容时仰视容量瓶刻度线;
D.定容时加水超过了刻度线,马上用胶头滴管吸去多余的水;
E.配制好后,发现称量是所用的托盘天平的砝码生锈了.
分析 (1)依据配制一定物质的量浓度溶液一般步骤选择需要仪器,依据配制溶液体积选择容量瓶规格;
(2)依据m=CVM计算需要氢氧化钠的质量;依据定容正确操作方法解答;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容等用到的仪器:托盘天平、小烧杯、钥匙、胶头滴管、玻璃棒、量筒、试剂瓶、容量瓶,配制95mL1mol/L NaOH溶液,需要选择100mL容量瓶,所以还缺少的仪器:100mL容量瓶;
故答案为:100mL容量瓶;
(2)配制95mL1mol/L NaOH溶液,需要选择100mL容量瓶,实际配制100mL溶液,需要氢氧化钠质量m=1mol/L×40g/mol×0.1L=4.0g;
定容时,将蒸馏水注入容量瓶,至液面距容量瓶颈刻度线下1-2cm时,改用胶头滴管滴加蒸馏水至刻度线;
故答案为:4.0;1-2cm;
(3)A.固体氢氧化钠溶解时未冷却至室温,就开始转移、洗涤以及定容,冷却后溶液体积偏小,溶液浓度偏高,故A选;
B.转移时不小心有少量溶液流到了容量瓶外,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故B不选;
C.定容时仰视容量瓶刻度线,导致溶液体积偏大,溶液浓度偏低,故C不选;
D.定容时加水超过了刻度线,马上用胶头滴管吸去多余的水,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故D不选;
E.配制好后,发现称量是所用的托盘天平的砝码生锈了,称取的氢氧化钠质量偏大,溶质的物质的量偏大,溶液浓度偏高,故E选;
故选:AE.
点评 本题考查了配制一定物质的量浓度的溶液的方法,明确原理,熟悉配置步骤和仪器的使用是解题关键,注意误差分析方法,侧重考查学生实验能力和分析能力.

 灵星计算小达人系列答案
灵星计算小达人系列答案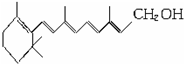 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 能被氧化为酮 | |
| B. | 维生素A是一种易溶于水的不饱和醇 | |
| C. | 维生素A的分子式为C20H32O | |
| D. | 维生素A分子中有异戊二烯的碳链结构 |
| A. | Na→Na2O2 | B. | SO2→S | C. | HCl→NaCl | D. | NaHCO3→CO2 |
| A. | Mg、Mg | B. | Mg、Al | C. | Al、Mg | D. | Al、Al |
| A. | 1 mol OT-含有的质子数、中子数均为10NA | |
| B. | 25℃,101kPa时,4.90LNH3含有的分子数约为0.2NA | |
| C. | 常温常压下,6g二氧化硅中所含硅氧键数目为0.2NA | |
| D. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
 CaCO3与稀盐酸反应(放热反应),CaCO3+2HCl=CaCl2+CO2↑+H2O,生成CO2的量与反应时间的关系如图所示,下列结论不正确的是( )
CaCO3与稀盐酸反应(放热反应),CaCO3+2HCl=CaCl2+CO2↑+H2O,生成CO2的量与反应时间的关系如图所示,下列结论不正确的是( )| A. | 反应开始2min内平均反应速率最大 | |
| B. | 可用c(Ca2+)或c(H+)的变化表示该反应速率 | |
| C. | 反应4min后平均反应速率减小 | |
| D. | 反应在第2min到第4min间生成CO2的平均反应速率为v${\;}_{C{O}_{2}}$=0.1mol/min |
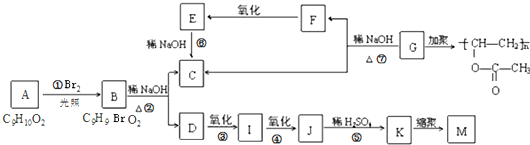
 .
.