题目内容
17.X、Y是短周期元素,两者组成化学式为X2Y2的化合物,已知X的原子序数为n,则Y的原子序数可能是( )(1)n+3(2)n-3(3)n+5(4)n-5(5)n+11.
| A. | (1)(2)(3) | B. | (2)(4) | C. | (1)(4)(5) | D. | 全部 |
分析 常见化学式为X2Y2的化合物,有H2O2、Na2O2、C2H2等,结合对应元素的元素序数解答该题.
解答 解:化学式为X2Y2的化合物,可能是钠与氧,氢与氧,碳与氢,X的原子序数为n,如果是Na2O2,则Y的原子序数n-3;如果是H2O2,则Y的原子序数n+7;如是C2H2,则Y的原子序数n-5,题中只有(2)(4)符合.
故选B.
点评 本题考查化合价与化学式及核电荷数的关系,为高频考点,把握常见的化合物中的元素的化合价及元素的核电荷数的关系为解答的关键,能利用举例的方法或价序原则来分析解答,题目难度不大.

练习册系列答案
相关题目
13.下列做法错误的是( )
| A. | 易燃试剂与强氧化性试剂分开放置并远离火源 | |
| B. | 向试管中滴加液体时,胶头滴管不能伸入试管 | |
| C. | 将FeCl3饱和溶液滴入热的稀氢氧化钠溶液中制备氢氧化铁胶体 | |
| D. | 金属钠着火时,用干燥的沙土覆盖灭火 |
14.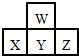 如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
 如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )| A. | 原子半径的大小顺序是Z>Y>X>W | |
| B. | Z的气态氢化物比X的气态氢化物稳定 | |
| C. | X、Y、Z各元素最高价和最低价的绝对值之和为8 | |
| D. | X、Y、Z最高价氧化物对应水化物的酸性强弱关系Z>Y>X |
5.下列物质中含有某些杂质(括号中),关于除杂质所用试剂及离子方程式均正确的是( )
| 加入试剂 | 对应化学或离子方程式 | ||
| A | 乙烷(乙烯) | 氢气 | CH2=CH2+H2$→_{加热}^{Ni}$CH3CH3 |
| B | CH3COOC2H5(CH3COOH) | NaOH溶液 | CH3COOH+NaOH=CH3COONa+H2O |
| C | MgCl2( FeCl3) | 氨水 | Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ |
| D | Fe2+(Fe3+) | Fe粉 | 2Fe3++Fe=3Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
12.以酚酞试液为指示剂,对某新制的NaOH溶液进行中和滴定试验,数据记录如下表:
该新制的NaOH溶液的浓度c (mol/L)合理的是( )
| 待测液 | 消耗标准盐酸(0.1000mol/L)的体积 | |
| ① | 20.00mL NaOH溶液 | V1 mL |
| ② | 20.00mL NaOH溶液+10.00mL水 | V2 mL |
| ③ | 敞口隔夜放置的20.00mL NaOH溶液 | V3 mL |
| A. | c=0.1000×$\frac{{V}_{1}+{V}_{2}+{V}_{3}}{3×20.00}$ | B. | c=0.1000×$\frac{{V}_{1}+{V}_{2}}{2×20.00}$ | ||
| C. | c=0.1000×$\frac{{V}_{1}+{V}_{3}}{2×20.00}$ | D. | c=$\frac{0.1000{V}_{1}}{20.00}$ |
6.在下列溶液中,能大量共存的一组离子是( )
| A. | pH=1的溶液中,NH4+、Fe3+、SO42-、Cl- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、SO42- | |
| D. | 由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- |
7.将纯锌片和纯铜片按如图所示方式插入同浓度的稀硫酸中,以下叙述正确的是( )
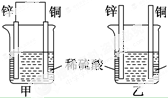

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 甲、乙中SO${\;}_{4}^{2-}$都向铜片移动 | D. | 产生气泡的速率甲中比乙中快 |
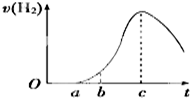 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示.
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示.