题目内容
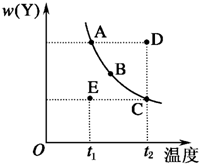 对于2X(g)?Y(g)的反应体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态).
对于2X(g)?Y(g)的反应体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态).(1)该反应的正反应方向是一个
(2)A、B、C、D、E各状态中,v(正)<v(逆)的是
(3)维持t1不变,E→A所需时间为x,维持t2不变,D→C所需时间为y,则x
(4)欲要求E状态从水平方向到C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是
考点:体积百分含量随温度、压强变化曲线,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)升高温度,平衡向吸热反应方向移动,根据升高温度Y百分含量的变化确定正反应是放热反应还是吸热反应;
(2)D点要达平衡,必须降低Y的百分含量,也就是逆向建立平衡,E点要到达平衡,必须升高Y的百分含量,正向建立平衡,A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等;
(3)温度越高反应速率越大,反应达到平衡时间越短;
(4)从当快速升温的瞬间,平衡未移动,但温度迅速升高,反映在图象上就是纵坐标不变,横坐标突然增大;当缓慢降温时,平衡不断地被破坏,但又不断地建立新的平衡.
(2)D点要达平衡,必须降低Y的百分含量,也就是逆向建立平衡,E点要到达平衡,必须升高Y的百分含量,正向建立平衡,A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等;
(3)温度越高反应速率越大,反应达到平衡时间越短;
(4)从当快速升温的瞬间,平衡未移动,但温度迅速升高,反映在图象上就是纵坐标不变,横坐标突然增大;当缓慢降温时,平衡不断地被破坏,但又不断地建立新的平衡.
解答:
解:(1)根据图象知,升高温度,Y的含量减少,说明平衡向逆反应方向移动,所以逆反应是吸热反应,则正反应是放热反应;
故答案为:放热;
(2)A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等,D点要达平衡,必须降低Y的百分含量,也就是逆向建立平衡,从而得出v(正)<v(逆),E点要达平衡,必须提高Y的百分含量,也就是正向建立平衡,从而得出v(正)>v(逆);
故答案为:D;
(3)温度越高反应速率越大,反应达到平衡时间越短,因为t1<t2,所以x>y,
故答案为:>;
(4)从当快速升温的瞬间,平衡未移动,但温度迅速升高,反映在图象上就是纵坐标不变,横坐标突然增大;当缓慢降温时,平衡不断地被破坏,但又不断地建立新的平衡,所以缓慢降温时,Y的体积百分含量的变化应不断地在平衡曲线上滑动.所以“使E状态从水平方向到达C状态”,应突然升温;“由C沿平衡曲线以达A状态”,应缓慢降温;
故答案为:先突然升温到t2,然后无限缓慢地降低温度到t1.
故答案为:放热;
(2)A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等,D点要达平衡,必须降低Y的百分含量,也就是逆向建立平衡,从而得出v(正)<v(逆),E点要达平衡,必须提高Y的百分含量,也就是正向建立平衡,从而得出v(正)>v(逆);
故答案为:D;
(3)温度越高反应速率越大,反应达到平衡时间越短,因为t1<t2,所以x>y,
故答案为:>;
(4)从当快速升温的瞬间,平衡未移动,但温度迅速升高,反映在图象上就是纵坐标不变,横坐标突然增大;当缓慢降温时,平衡不断地被破坏,但又不断地建立新的平衡,所以缓慢降温时,Y的体积百分含量的变化应不断地在平衡曲线上滑动.所以“使E状态从水平方向到达C状态”,应突然升温;“由C沿平衡曲线以达A状态”,应缓慢降温;
故答案为:先突然升温到t2,然后无限缓慢地降低温度到t1.
点评:本题考查化学平衡图象问题,题目难度中等,本题注意把握图象曲线的特点以及温度对平衡移动的影响.

练习册系列答案
相关题目
如图所示的五中元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22,下列说法正确的是( )
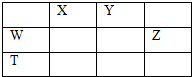

| A、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B、由X、Y和氢三种元素形成的化合物中只有共价键 |
| C、物质WY2,W3X4,WZ4均有熔点高,硬度大的特性 |
| D、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
下列说法正确的是( )
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A、该反应的正反应为放热反应 |
| B、达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小 |
| C、容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的长 |
| D、若起始时向容器Ⅰ中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行 |
某溶液仅含K+、NH4+、Al3+、Fe2+、Mg2+、Ba2+、Cl-、NO3-、CO32-、SO42-中的4种离子,且所含离子的物质的量均为1mol.化学兴趣小组把溶液均匀分成四份,分别取样品进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
| A、该溶液中所含的离子是:Fe2+、K+、SO42-、NO3- |
| B、实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为18g |
| C、若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D、若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液会显血红色 |
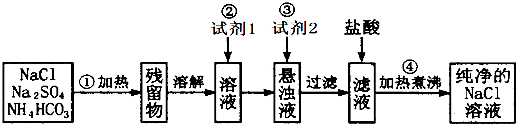
 某地区使用含较多Ca2+、Mg2+的天然水按下列步骤制取纯净水.
某地区使用含较多Ca2+、Mg2+的天然水按下列步骤制取纯净水.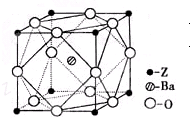 Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知:
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素.已知: