题目内容
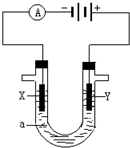
 金属腐蚀的电化学原理可用如图模拟.
金属腐蚀的电化学原理可用如图模拟.(1)请写出有关电极反应式:
①铁棒上的电极反应式:
②碳棒上的电极反应式:
(2)该图所表示的是
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)图示为Fe的吸氧腐蚀,负极上Fe失电子生成亚铁离子,正极上氧气得电子生成氢氧根离子;
(2)在NaCl溶液中发生吸氧腐蚀;
(3)将NaCl溶液改为稀H2SO4溶液,变成析氢腐蚀;保护铁棒时,负极应为比铁活泼的金属.
(2)在NaCl溶液中发生吸氧腐蚀;
(3)将NaCl溶液改为稀H2SO4溶液,变成析氢腐蚀;保护铁棒时,负极应为比铁活泼的金属.
解答:
解:(1)图示为Fe的吸氧腐蚀,负极上Fe失电子生成亚铁离子,正极上氧气得电子生成氢氧根离子,
①铁棒上的电极反应式为:2Fe-4e-═2Fe2+,故答案为:2Fe-4e-═2Fe2+;
②碳棒上的电极反应式为:O2+2H2O+4e-═4OH-,故答案为:O2+2H2O+4e-═4OH-;
(2)在NaCl溶液中发生吸氧腐蚀,故答案为:吸氧;
(3)将NaCl溶液改为稀H2SO4溶液,变成析氢腐蚀;保护铁棒时,负极应为比铁活泼的金属,故答案为:析氢;锌(或其他比铁活泼的金属).
①铁棒上的电极反应式为:2Fe-4e-═2Fe2+,故答案为:2Fe-4e-═2Fe2+;
②碳棒上的电极反应式为:O2+2H2O+4e-═4OH-,故答案为:O2+2H2O+4e-═4OH-;
(2)在NaCl溶液中发生吸氧腐蚀,故答案为:吸氧;
(3)将NaCl溶液改为稀H2SO4溶液,变成析氢腐蚀;保护铁棒时,负极应为比铁活泼的金属,故答案为:析氢;锌(或其他比铁活泼的金属).
点评:本题考查了金属的腐蚀和防护,注意吸氧腐蚀和析氢腐蚀的区别,题目难度不大.

练习册系列答案
 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
已知CH3COOH?CH3COO-+H+,下列不能说明CH3COOH是弱酸的是( )
| A、用醋酸除去水壶中的水垢 |
| B、0.01mol/LCH3COOH的pH>2 |
| C、常温下,CH3COONa溶液的pH>7 |
| D、滴有石蕊溶液的CH3COOH溶液变红,加入少量的CH3COONH4固体,溶液的颜色变浅 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质下列说法正确的是( )
| A、糖类、油脂、蛋白质都能发生水解反应,其中油脂在碱性条件下的水解称为皂化反应 |
| B、淀粉和纤维素互为同分异构体,都能水解为还原性的糖 |
| C、糖类、油脂、蛋白质都是高分子化合物 |
| D、植物油能使溴的四氯化碳溶液褪色 |
下列物质中,属于天然高分子化合物的是( )
| A、脂肪 | B、淀粉 |
| C、麦芽糖 | D、聚氯乙烯 |
波尔多液农药不能用铁制容器盛放,是因为铁能与农药中的硫酸铜反应.在该反应中铁( )
| A、是催化剂 | B、得到电子 |
| C、是还原剂 | D、发生了还原反应 |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有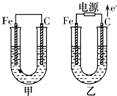 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
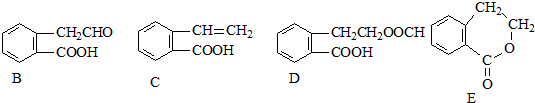
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题: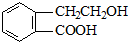 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.