题目内容
几种离子化合物组成的混合物,含以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、Cl-、NO2-、SO42-、CO32-.将该混合物溶于水后得澄清溶液,现取4份100mL该溶液分别进行如下实验:
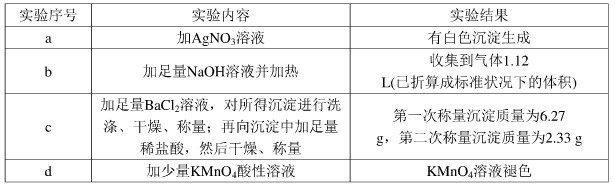
试回答下列问题:
(1)根据实验a判断Cl-是否存在 (填“一定存在”、“一定不存在”或“不能确定”).
(2)该混合物中一定不存在的离子是 .
(3)①写出实验b中发生反应的离子方程式 .
②写出实验d中使KMnO4酸性溶液褪色的离子方程式 .
(4)溶液中一定存在的阴离子及其物质的量浓度为(可不填满):
(5)混合物中是否存在K+? ,判断的理由是 .

试回答下列问题:
(1)根据实验a判断Cl-是否存在
(2)该混合物中一定不存在的离子是
(3)①写出实验b中发生反应的离子方程式
②写出实验d中使KMnO4酸性溶液褪色的离子方程式
(4)溶液中一定存在的阴离子及其物质的量浓度为(可不填满):
| 阴离子符号 | 物质的量浓度(mol?L-1) |
考点:常见离子的检验方法,常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题,离子反应专题
分析:a.加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
b.1.12L为氨气,氨气的物质的量为0.05mol,溶液中一定含有NH4+,并且物质的量为0.05mol;
c.2.33g为硫酸钡,碳酸钡的物质的量为0.01mol;6.27g为硫酸钡和碳酸钡,碳酸钡的质量为:6.27g-2.33g=3.94g,物质的量为0.02mol;溶液中一定存SO42-、CO32-,根据离子共存可知,一定不存在Mg2+、Ba2+;
d.加入少量的酸性高锰酸钾溶液,高锰酸钾溶液褪色,说明溶液中含有还原性离子NO2-,
再根据电荷守恒,判断是否存在钾离子,据此进行解答.
b.1.12L为氨气,氨气的物质的量为0.05mol,溶液中一定含有NH4+,并且物质的量为0.05mol;
c.2.33g为硫酸钡,碳酸钡的物质的量为0.01mol;6.27g为硫酸钡和碳酸钡,碳酸钡的质量为:6.27g-2.33g=3.94g,物质的量为0.02mol;溶液中一定存SO42-、CO32-,根据离子共存可知,一定不存在Mg2+、Ba2+;
d.加入少量的酸性高锰酸钾溶液,高锰酸钾溶液褪色,说明溶液中含有还原性离子NO2-,
再根据电荷守恒,判断是否存在钾离子,据此进行解答.
解答:
解:(1)与AgNO3溶液有沉淀产生的离子有:Cl-、CO32-、SO42-,根据a无法确定是否含有氯离子,
故答案为:不能确定;
(2)根据c可知,溶液中一定存在SO42-、CO32-,则一定不存在与SO42-、CO32-反应的离子:Mg2+、Ba2+,
故答案为:Mg2+、Ba2+;
(3)①实验b加足量NaOH溶液加热产生气体,气体是氨气,反应的离子方程式为:NH4++OH-
NH3↑+H2O,
故答案为:NH4++OH-
NH3↑+H2O;
②酸性高锰酸钾溶液能够将NO2-氧化成硝酸根离子,反应的离子方程式为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O,
故答案为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O;
(4)不溶于盐酸的2.33g沉淀为硫酸钡,物质的量是0.01mol,浓度为:c(CO32-)=
=0.1mol/L;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g-2.33g=3.94g,物质的量为0.02mol,硫酸根离子浓度为:c(SO42-)=
=0.2mol/L;根据d可知,一定存在,NO2-,但是无法确定其物质的量及浓度,
故答案为:
;
(5)实验b中收集的1.12L气体为氨气,氨气的物质的量为0.05mol,则溶液中一定含有NH4+,物质的量为0.05mol;再根据实验测定可知,溶液中一定存在的离子是NO2-、SO42-、CO32-,经计算,碳酸根离子为0.01mol,硫酸根离子为0.02mol,根据电荷守恒,n(+)=n(NH4+)=0.05mol,c(-)=2n(CO32-)+2n(SO42-)=0.06mol,钾离子一定存在,
故答案为:存在;通过实验可知溶液中一定存在的离子是NH4+、NO2-、SO42-、CO32-,经计算,铵根离子的物质的量为0.05mol,碳酸根离子为0.01mol,硫酸根离子为0.02mol,根据电荷守恒,n(+)=n(NH4+)=0.05mol,c(-)=2n(CO32-)+2n(SO42-)=0.06mol,钾离子一定存在.
故答案为:不能确定;
(2)根据c可知,溶液中一定存在SO42-、CO32-,则一定不存在与SO42-、CO32-反应的离子:Mg2+、Ba2+,
故答案为:Mg2+、Ba2+;
(3)①实验b加足量NaOH溶液加热产生气体,气体是氨气,反应的离子方程式为:NH4++OH-
| ||
故答案为:NH4++OH-
| ||
②酸性高锰酸钾溶液能够将NO2-氧化成硝酸根离子,反应的离子方程式为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O,
故答案为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O;
(4)不溶于盐酸的2.33g沉淀为硫酸钡,物质的量是0.01mol,浓度为:c(CO32-)=
| 0.01mol |
| 0.1L |
| 0.02mol |
| 0.1L |
故答案为:
| 阴离子符号 | 物质的量浓度(mol?L-1) |
| SO42- | 0.1 |
| CO32- | 0.2 |
| NO2- | - |
(5)实验b中收集的1.12L气体为氨气,氨气的物质的量为0.05mol,则溶液中一定含有NH4+,物质的量为0.05mol;再根据实验测定可知,溶液中一定存在的离子是NO2-、SO42-、CO32-,经计算,碳酸根离子为0.01mol,硫酸根离子为0.02mol,根据电荷守恒,n(+)=n(NH4+)=0.05mol,c(-)=2n(CO32-)+2n(SO42-)=0.06mol,钾离子一定存在,
故答案为:存在;通过实验可知溶液中一定存在的离子是NH4+、NO2-、SO42-、CO32-,经计算,铵根离子的物质的量为0.05mol,碳酸根离子为0.01mol,硫酸根离子为0.02mol,根据电荷守恒,n(+)=n(NH4+)=0.05mol,c(-)=2n(CO32-)+2n(SO42-)=0.06mol,钾离子一定存在.
点评:本题考查了常见离子的检验方法,题目难度较大,题量较大,试题涉及了常见离子的检验方法判断、离子方程式的书写,题中根据电荷守恒判断钾离子的存在为难点和易错点.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
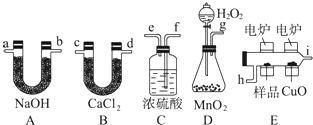
下列有关实验原理、装置、操作或结论的描述中,正确的是( )


| A、图①装置的烧杯中先出现白色沉淀后溶解 |
| B、图②装置可验证氧化性:ClO->Cl2>Fe3+ |
| C、图③装置可用于实验室制备乙烯 |
| D、图④装置可证明Na2CO3比NaHCO3更稳定 |
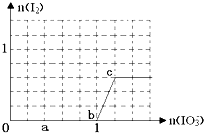 已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )
已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )| A、0-b:3HSO3-+IO3-═3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2mol |
| C、b-c间I2是还原产物 |
| D、当溶液中I?与I2的物质的量之比为5:2时,加入的KIO3为1.08mol |
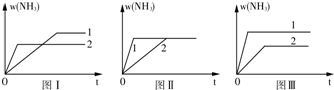
已知:4NH3+5O2=4NO+6H2O,若反应速率分别用v NH3、v O2、vNO、v H2O(mol/L?min)表示,则正确的关系是( )
A、
| ||
B、
| ||
C、
| ||
D、
|