题目内容
8.唐山市曹妃甸区10月20日的空气质量日报如表:| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫 | 6 | ||
| 二氧化氮 | 20 |
| A. | 用氢气作燃料 | B. | 露天焚烧垃圾 | ||
| C. | 大量排放汽车尾气 | D. | 用煤作燃料 |
分析 本题要根据空气质量每周公报的部分内容,判断产物对空气是否造成污染.表中说明可吸入颗粒、二氧化硫、二氧化氮都是空气污染物.
解答 解:A.氢气燃烧生成产物为水,没有表中的项目,对表中三个空气质量指标不会产生影响,故A正确;
B.垃圾燃烧会产生大量的可吸入颗粒和有害气体,含有表中项目,故B错误;
C.汽车排放的尾气还有较多的二氧化氮等有害物质,含表中项目,故C错误;
D.煤和燃烧会有二氧化硫生成,含表中项目,故D错误;
故选:A.
点评 本题考查了生活中常见的环境污染与治理,熟悉相关物质的性质是解题关键,有助于养成爱护环境,节能减排的习惯,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.关于焰色反应实验,说法错误的是( )
| A. | 做焰色反应实验用的铂丝要用受热容易挥发的稀盐酸洗涤 | |
| B. | 观察K2SO4的焰色应透过蓝色的钴玻璃 | |
| C. | 可以用焰色反应来区别NaCl溶液和KCl溶液 | |
| D. | 焰色反应一定是化学变化 |
19.下面有关氧化还原反应的叙述正确的是( )
| A. | 在反应中不一定所有元素的化合价都发生变化 | |
| B. | 肯定有一种元素被氧化,另一种元素被还原 | |
| C. | 非金属单质在反应中只做氧化剂 | |
| D. | 某元素从化合物变为单质时,该元素一定被还原 |
16.需要加入氧化剂才能实现的变化是( )
| A. | MnO2→MnSO4 | B. | KI→KIO3 | C. | HNO 3→NO | D. | Al2O 3→Al(OH)3 |
13. 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:
(1)常温下,若三者体积均为200mL 浓度均为0.1mol•L-1,则三者中C(H+)最小的是次氯酸(填名称).
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
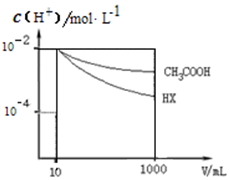
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.
 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.
17.某反应CH3OH(l)+NH3(g)?CH3NH2(g)+H2O(g)在高温度时才能自发进行,则该反应过程的△H、△S判断正确的是( )
| A. | △H>0、△S<0 | B. | △H>0、△S>0 | C. | △H<0、△S<0 | D. | △H<0、△S>0 |
19.某学生用0.1000mol•L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)ABDCEF.
(2)上述B步骤操作的目的是除去附在滴定管壁上的水,防止水稀释标准溶液.
(3)实验中用左手控制活塞,眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.判断到达终点的现象是溶液的颜色由无色变浅红且保持半分钟内不褪色.
(4)某学生根据3次实验分别记录有关数据如表:
依据上表数据列式计算该盐酸溶液的物质的量浓度为
(5)用0.1000mol•L-1 NaOH溶液滴定0.1000mol•L-1盐酸,如达到滴定的终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05mL),继续加水至50mL,所得溶液的pH等于10
(6)下列哪些操作会使测定结果偏高B、C、E(填序号).
A.锥形瓶中溶液的颜色刚刚由无色变为浅红色即停止滴定
B.碱式滴定管用蒸馏水洗净后立即注入标准液
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
E.实验中,用待盛装的溶液润洗锥形瓶.
A.移取20mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)ABDCEF.
(2)上述B步骤操作的目的是除去附在滴定管壁上的水,防止水稀释标准溶液.
(3)实验中用左手控制活塞,眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.判断到达终点的现象是溶液的颜色由无色变浅红且保持半分钟内不褪色.
(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测溶液的体积(mL) | 0.100 0mol•L-1NaOH的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积(mL) | ||
| 第一次 | 20.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 20.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 20.00 | 0.22 | 26.31 | 26.09 |
(5)用0.1000mol•L-1 NaOH溶液滴定0.1000mol•L-1盐酸,如达到滴定的终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05mL),继续加水至50mL,所得溶液的pH等于10
(6)下列哪些操作会使测定结果偏高B、C、E(填序号).
A.锥形瓶中溶液的颜色刚刚由无色变为浅红色即停止滴定
B.碱式滴定管用蒸馏水洗净后立即注入标准液
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
E.实验中,用待盛装的溶液润洗锥形瓶.
