题目内容
短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A、B与A只能组成BA3化合物 |
| B、C、D、E形成的化合物与稀硫酸可能发生氧化还原反应 |
| C、A、B、C形成的化合物一定不能发生水解反应 |
| D、E的氧化物对应的水化物一定有强的氧化性 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期中的A、B、C、D、E五种元素,原子序数依次增大,C2-与D+的核外电子数相等,结合所带电荷可知,C为O元素、D为Na;A和D,A为非金属元素,则A为H元素;C和E分别同主族,E为S元素;A与B的原子序数之和等于C的原子序数,则B的原子序数=8-1=7,故B为N元素,据此解答.
解答:
解:短周期中的A、B、C、D、E五种元素,原子序数依次增大,C2-与D+的核外电子数相等,结合所带电荷可知,C为O元素、D为Na;A和D,A为非金属元素,则A为H元素;C和E分别同主族,E为S元素;A与B的原子序数之和等于C的原子序数,则B的原子序数=8-1=7,故B为N元素,
A.N与H元素可以形成NH3、N2H4等,故A错误;
B.O、Na、S形成的化合物Na2S2O3,可与稀硫酸发生氧化还原反应,故B正确;
C.H、N、O形成的化合物NH4NO3能发生水解反应,故C错误;
D.亚硫酸、稀硫酸没有强氧化性,浓硫酸具有强氧化性,故D错误,
故选B.
A.N与H元素可以形成NH3、N2H4等,故A错误;
B.O、Na、S形成的化合物Na2S2O3,可与稀硫酸发生氧化还原反应,故B正确;
C.H、N、O形成的化合物NH4NO3能发生水解反应,故C错误;
D.亚硫酸、稀硫酸没有强氧化性,浓硫酸具有强氧化性,故D错误,
故选B.
点评:本题考查结构性质位置关系应用,推断元素是解题的关键,C2-与D+的核外电子数相等是推断突破口,B选项为易错点,难度中等.

练习册系列答案
相关题目
元素X、Y可形成XY2型离子化合物,它们的原子序数可能为( )
| A、6,8 | B、12,9 |
| C、16,8 | D、11,16 |
常温下,0.1mol/L某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol/L |
| B、溶液中c(H+)+c(A-)=0.1mol/L |
| C、溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大 |
| D、与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为 c(A-)>c(Na+)>c(OH-)>c(H+) |
下列物质中,作为燃料燃烧时对空气无污染的是( )
| A、汽油 | B、煤 | C、沼气 | D、氢气 |
已知:H-H、Cl-Cl、H-Cl的键能分别为436kJ/mol、243kJ/mol和431kJ/mol,估计1molCl2和1molH2完全反应生成2molHCl的反应热为( )
| A、-183 kJ/mol |
| B、-91.5 kJ/mol |
| C、+183 kJ/mol |
| D、+91.5 kJ/mol |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
| A、增加压强 |
| B、升高温度 |
| C、增大CO 的浓度 |
| D、更换催化剂 |
对于电解质溶液,下列说法不正确的是( )
| A、常温下,pH=2的氯水中:c(Cl-)+c(ClO-)+c(OH-)=0.01mol/L |
| B、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| C、MgCO3可以除去MgCl2酸性溶液中的Fe3+ |
| D、在pH=1的溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
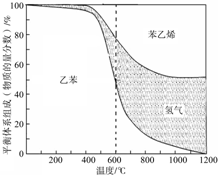 苯乙烯是重要的基础有机原料.工业中用乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:
苯乙烯是重要的基础有机原料.工业中用乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:
