题目内容
下列说法错误的是( )
| A、Na2SO3溶液与BaCl2溶液混合有白色沉淀生成,加稀HNO3沉淀不消失 |
| B、将SO2气体通入足 量Ba(OH)2溶液中有白色沉淀生成,加足 量HCl后沉淀消失 |
| C、将SO2气体通入BaCl2溶液中有白色沉淀生成,加稀HCl后沉淀消失 |
| D、将SO2气体通入氯水中无沉淀生成,加入BaCl2溶液有白色沉淀生成 |
考点:含硫物质的性质及综合应用,二氧化硫的化学性质
专题:元素及其化合物
分析:A、硝酸具有强氧化性,能氧化+4价的S元素生成硫酸根,据此分析;
B、二氧化硫为酸性气体,与碱反应生成亚硫酸盐(亚硫酸钡),亚硫酸钡溶于稀盐酸,据此分析;
C、二氧化硫与氯化钡不反应,据此分析;
D、氯水具有强化化性,能氧化+4价S生成硫酸根,据此分析.
B、二氧化硫为酸性气体,与碱反应生成亚硫酸盐(亚硫酸钡),亚硫酸钡溶于稀盐酸,据此分析;
C、二氧化硫与氯化钡不反应,据此分析;
D、氯水具有强化化性,能氧化+4价S生成硫酸根,据此分析.
解答:
解:A、硝酸具有强氧化性,能氧化+4价的S元素生成硫酸根,硫酸根与钡离子生成硫酸钡沉淀,故A正确啊;
B、二氧化硫为酸性气体,与碱反应生成亚硫酸盐(亚硫酸钡难溶于水),亚硫酸钡溶于稀盐酸,故B正确;
C、二氧化硫与氯化钡不反应,故C错误;
D、氯水具有强化化性,能氧化+4价S生成硫酸根,硫酸根与钡离子生成硫酸钡沉淀,故D正确,故选C.
B、二氧化硫为酸性气体,与碱反应生成亚硫酸盐(亚硫酸钡难溶于水),亚硫酸钡溶于稀盐酸,故B正确;
C、二氧化硫与氯化钡不反应,故C错误;
D、氯水具有强化化性,能氧化+4价S生成硫酸根,硫酸根与钡离子生成硫酸钡沉淀,故D正确,故选C.
点评:本题主要考查的是+4价硫的还原性、钡盐的性质等,综合性较强,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列能用或图装置制取气体并能“随开随用、随关随停”的是( )
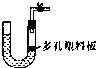

| A、锌粒和稀硫酸制取氧气 |
| B、电石和水制取乙炔 |
| C、浓盐酸和二氧化锰制取氯气 |
| D、大理石和稀硫酸制取二氧化碳 |
下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.相同条件下,有关上述溶液的比较中,正确的是( )
| A、由水电离的c(H+):①=②>③=④ |
| B、将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②>③ |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D、向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>② |
在溶液中能与Fe3+共存的微粒是( )
| A、Cu |
| B、S2- |
| C、CO32- |
| D、Fe2+ |
下列关于有机物的叙述正确的是( )
| A、所有含碳元素的化合物都是有机物 |
| B、大多数有机物难溶于有机溶剂 |
| C、熔点低的化合物是有机物 |
| D、有机物中除含碳元素外,还常含有氢、氧等元素 |
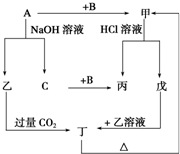 由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答:
由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答: 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组设计的实验装置图如图.请回答相关问题:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组设计的实验装置图如图.请回答相关问题: