题目内容
6.在恒温恒容的密闭容器中,反应SO2+NO2?NO+SO3建立了化学平衡,此时若在容器中再通入一定量的O2,反应将会发生的变化是( )| A. | 平衡向正反应方向移动 | B. | 平衡将向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 容器内气体的密度不变 |
分析 反应SO2(g)+NO2(g)?NO(g)+SO3(g),达到平衡状态后,加入一定量的氧气,氧气与一氧化氮反应生成了二氧化氮,导致一氧化氮浓度减小,二氧化氮浓度增大,所以化学平衡向着正向移动,据此进行判断.
解答 解:由于反应SO2(g)+NO2(g)?NO(g)+SO3(g),达到平衡状态后,加入一定量的氧气,氧气与一氧化氮反应生成了二氧化氮,导致一氧化氮浓度减小,二氧化氮浓度增大,所以化学平衡向着正向移动,充入氧气,气体的质量增大、体积不变,所以容器内气体的密度增大,
故选A.
点评 本题考查了化学平衡的影响因素,注意分析题中信息,根据平衡移动原理进行分析,题目较简单.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
16.已知Zn(s)+H2SO4(sq)═ZnSO4(aq)+H2(g)△H<0,则下列叙述不正确的是( )
| A. | 该反应的化学能可以转化为电能 | |
| B. | 该反应的△H值与反应方程式的化学计量数有关 | |
| C. | 该反应的反应物的总能量高于生成物的总能量 | |
| D. | 该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量 |
14.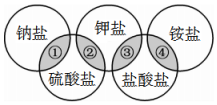 下列各项中的物质,能满足图中阴影部分关系的是( )
下列各项中的物质,能满足图中阴影部分关系的是( )
 下列各项中的物质,能满足图中阴影部分关系的是( )
下列各项中的物质,能满足图中阴影部分关系的是( )| 物质 选项 | ① | ② | ③ | ④ |
| A | NaCl | KCl | K2SO4 | NH4Cl |
| B | Na2SO4 | K2SO4 | KCl | NH4Cl |
| C | NaCl | KCl | NH4Cl | K2SO4 |
| D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
| A. | A | B. | B | C. | C | D. | D |
11.下列变化中,属于物理变化的是( )
| A. | 熔融态的KCl导电 | |
| B. | 在Fe(OH)3胶体中加入MgSO4溶液析出红褐色沉淀 | |
| C. | 用加热方法分离沙子和NH4Cl晶体 | |
| D. | 蓝色CuSO4晶体,受热变为白色CuSO4粉末 |
18.硅及其化合物在工农业生产及科技等方面用途广泛.其中不正确的是( )
| A. | 二氧化硅在地壳中含量丰富,广泛用于制造水泥、玻璃、陶瓷等 | |
| B. | 硅酸钠在建筑工业上常用作黏合剂和木材防火剂 | |
| C. | 碳化硅的结构与金刚石相似,硬度很大常用做砂轮和砂纸 | |
| D. | 硅是良好的半导体材料故用作光导纤维 |
3.工业上利用反应2FeSO4+NaBH4+4NaOH=2Fe+2H2↑+Na[B(OH)4]+2Na2SO4制取纳米铁,下列说法不正确的是( )
| A. | NaBH4与盐酸不反应 | |
| B. | NaBH4的电子式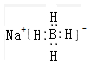 | |
| C. | 每生成1molFe,转移2mol电子 | |
| D. | 氧化产物与还原产物的物质的量之比为1:1 |
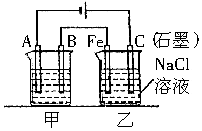 如图所示甲、乙为相互串联的两电解池.试回答:
如图所示甲、乙为相互串联的两电解池.试回答: