题目内容
下面是甲、乙、丙3位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关的实验任务
实验目的:制取乙酸乙酯
实验原理:甲、乙、丙3位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯.
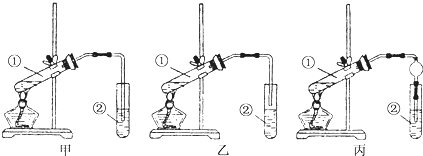
装置设计:甲、乙、丙3位同学分别设计了下列3套实验装置:
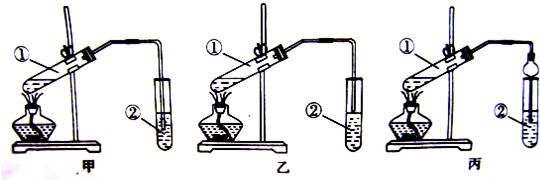
若从甲、乙两位同学设计的装置中选择1套作为实验室制取乙酸乙酯的装置,应该选择的装置是 (填“甲”或“乙”).丙同学将甲装置中的玻璃导管改成了球形干燥管,除起导气和冷凝作用外,另一个重要的作用是 .
实验步骤:
a.按所选择的装置组装仪器,在试管①中先加入3mL95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;
c.在试管②中加5mL饱和Na2CO3溶液;
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象停止实验.
问题讨论:
(1)步骤a中组装好实验装置后,加入样品前还应检查 .
(2)试管②中装有饱和Na2CO3溶液,其作用是 (填字母).
A.吸收乙醇 B.中和乙酸
C.乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)根据试管②中观察到的现象,可知乙酸乙酯的物理性质有 .
实验目的:制取乙酸乙酯
实验原理:甲、乙、丙3位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯.
装置设计:甲、乙、丙3位同学分别设计了下列3套实验装置:

若从甲、乙两位同学设计的装置中选择1套作为实验室制取乙酸乙酯的装置,应该选择的装置是
实验步骤:
a.按所选择的装置组装仪器,在试管①中先加入3mL95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;
c.在试管②中加5mL饱和Na2CO3溶液;
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象停止实验.
问题讨论:
(1)步骤a中组装好实验装置后,加入样品前还应检查
(2)试管②中装有饱和Na2CO3溶液,其作用是
A.吸收乙醇 B.中和乙酸
C.乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)根据试管②中观察到的现象,可知乙酸乙酯的物理性质有
考点:乙酸乙酯的制取
专题:实验题,有机化学基础
分析:装置中②的导管不能伸入液面以下,否则容易发生倒吸现象,则装置甲会发生倒吸现象,装置乙合理;丙中球形干燥管还可以防止倒吸;
(1)实验前,要检查装置的气密性;
(2)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
(3)根据试管②中观察到乙酸乙酯的颜色、状态、密度等方面进行解答.
(1)实验前,要检查装置的气密性;
(2)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
(3)根据试管②中观察到乙酸乙酯的颜色、状态、密度等方面进行解答.
解答:
解:乙酸和乙醇易溶于水,不插入液面下是为了防止倒吸,所以选乙装置;球形干燥管导气的同时也起到防倒吸作用,故答案为:乙;防止倒吸;
(1)实验前,要检查装置的气密性,否则会导致实验失败,
故答案为:装置气密性;
(2)碳酸钠溶液能够吸收乙醇,能跟乙酸反应中和乙酸,便于闻到乙酸乙酯的香味,且乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出,所以ABC正确;饱和碳酸钠溶液不影响乙酸乙酯的产率,故D错误,
故答案为:ABC;
(3)实验观察到盛放饱和碳酸钠溶液试管中溶液分层,无色油状液体在上等现象,说明乙酸乙酯物理性质有:无色油状液体、不溶于水、密度比水小,可以闻到香味,
故答案为:无色油状液体、不溶于水、密度比水小,可以闻到香味.
(1)实验前,要检查装置的气密性,否则会导致实验失败,
故答案为:装置气密性;
(2)碳酸钠溶液能够吸收乙醇,能跟乙酸反应中和乙酸,便于闻到乙酸乙酯的香味,且乙酸乙酯在饱和Na2CO3溶液中的溶解度更小,有利于分层析出,所以ABC正确;饱和碳酸钠溶液不影响乙酸乙酯的产率,故D错误,
故答案为:ABC;
(3)实验观察到盛放饱和碳酸钠溶液试管中溶液分层,无色油状液体在上等现象,说明乙酸乙酯物理性质有:无色油状液体、不溶于水、密度比水小,可以闻到香味,
故答案为:无色油状液体、不溶于水、密度比水小,可以闻到香味.
点评:本题考查了乙酸乙酯的制备方法,题目难度不大,注意掌握制取乙酸乙酯的反应原理及实验室的制备方法,明确浓硫酸、饱和碳酸钠溶液的作用,特别注意吸收乙酸乙酯的导管不能伸入液面以下,否则会发生倒吸现象.

练习册系列答案
相关题目
核电荷数为15的原子,n层电子个数最多,n层为( )
| A、K层 | B、N层 | C、M层 | D、L层 |
具有下列外围电子排布式的基态原子中,最容易形成离子的是( )
| A、3s23p1 |
| B、2s22p2 |
| C、3s2 |
| D、4s24p3 |
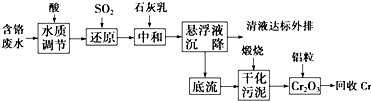 含铬废水、铬渣对环境的污染问题备受关注,通过化学原理对废物进行有效处理变废为宝是目前的一个重要研究课题.
含铬废水、铬渣对环境的污染问题备受关注,通过化学原理对废物进行有效处理变废为宝是目前的一个重要研究课题.