题目内容
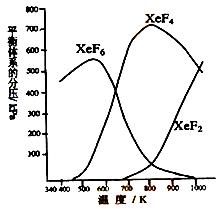
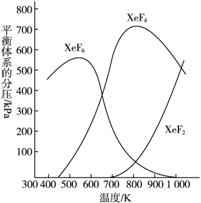
23.在密闭容器中,有一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如图所示(已知气体的分压之比等于物质的量之比)。
⑴ 420K时,发生反应的化学方程式为:____________________________,若反应中消耗1 mol Xe,则转移电子______mol。
⑵ 600~800K时,会发生反应:XeF6(g) ![]() XeF4(g) + F2(g),其反应热△H________0(填“>”、“=”或“<”),理由是__________________________________________。
XeF4(g) + F2(g),其反应热△H________0(填“>”、“=”或“<”),理由是__________________________________________。
⑶ 900K时,容器中存在的组分有_________________。
答案:
(1)Xe + 3 F2===== XeF6 6
(2)>
随着温度的升高,XeF6(g)![]() XeF4(g)+F2(g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的△H>0。
XeF4(g)+F2(g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的△H>0。
(3)XeF6、XeF4、XeF2、Xe、F2
解析:本题主要考查化学反应速率、化学平衡等知识,还涉及氧化还原反应中电子转移数目的计算、反应热ΔH的判定等。题目以看图设置情境设问,重点考查观察能力和思维能力。
(1)由图象可知,在420 K时,平衡体系中无XeF4、XeF2生成(二者分压为零),只有生成物XeF6,此时反应的化学方程式为![]() e+3
e+3![]() 2====
2====![]()
![]() 6。若反应中消耗1 mol Xe时,则转移电子6 mol。
6。若反应中消耗1 mol Xe时,则转移电子6 mol。
(2)在600~800 K时,反应XeF6(g)![]() XeF4(g)+F2(g)达平衡后,随着温度的升高,XeF6不断减少,XeF4不断增多,上述平衡向右移动,说明正反应为吸热反应,该反应的ΔH>0。
XeF4(g)+F2(g)达平衡后,随着温度的升高,XeF6不断减少,XeF4不断增多,上述平衡向右移动,说明正反应为吸热反应,该反应的ΔH>0。
(3)由图象可知,在900 K时,平衡体系中三种生成物XeF6、XeF4、XeF2都存在,又因为是可逆反应,还应有反应物Xe、F2存在。

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案
相关题目
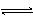 XeF4(g) + F2(g) , 其反应热
XeF4(g) + F2(g) , 其反应热