题目内容
将一定量的镁铝合金样品分成两等份,一份加入到足量的NaOH溶液中,充分反应后,收集到标准状况下气体6.72L;另一份加入到足量稀盐酸中,充分反应后,收集到标准状况下气体11.2L.则原合金样品中镁的质量为( )
| A、4.8 g |
| B、6 g |
| C、9.6 g |
| D、12 g |
考点:有关混合物反应的计算
专题:
分析:先根据第一份中发生的反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑计算出铝的物质的量,再根据第二份中发生反应2Al+6HCl═2AlCl3+3H2↑、Mg+2HCl═MgCl2+H2↑计算出每份混合物中镁的物质的量,再计算出原合金中镁的总物质的量及质量.
解答:
解:第一份中气体的物质的量为:
=0.3mol,
设铝的物质的量为x,则
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
x 0.3mol
则:3x=0.3mol×2,
解得:x=0.2mol,
第二份中气体的物质的量为:
=0.5mol,设镁的物质的量为y,
2Al+6HCl═2AlCl3+3H2↑
2 3
0.2mol 0.3mol
Mg+2HCl═MgCl2+H2↑
1 1
y (0.5mol-0.3mol)=0.2mol
y×1=1×0.2mol,
解得:y=0.2mol,即:每份混合物中含有0.2mol,0.2mol镁的质量为:24g/mol×0.2mol=4.8g,
所以原合金中含有镁的质量为:4.8g×2=9.6g,
故选C.
| 6.72L |
| 22.4L/mol |
设铝的物质的量为x,则
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
x 0.3mol
则:3x=0.3mol×2,
解得:x=0.2mol,
第二份中气体的物质的量为:
| 11.2L |
| 22.4L/mol |
2Al+6HCl═2AlCl3+3H2↑
2 3
0.2mol 0.3mol
Mg+2HCl═MgCl2+H2↑
1 1
y (0.5mol-0.3mol)=0.2mol
y×1=1×0.2mol,
解得:y=0.2mol,即:每份混合物中含有0.2mol,0.2mol镁的质量为:24g/mol×0.2mol=4.8g,
所以原合金中含有镁的质量为:4.8g×2=9.6g,
故选C.
点评:本题考查混合物反应的计算,题目难度中等,熟悉铝与碱反应而镁不与碱反应是解答本题的关键,需要明确本题求算的是原混合物中镁的总质量,而计算过程中的数据是分成两等份的,为易错点.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
对一个有气体参与的反应,下列能加快反应速率且不改变活化分子百分数的是( )
| A、定容容器中通入Ar |
| B、增大压强 |
| C、升温 |
| D、加入催化剂 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知C (石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| B、已知C (s)+O2(g)=CO2(g);△H1,C (s)+1/2O2(g)=CO(g);△H2,则△H2>△H1 |
| C、已知CH4 (g)+2O2(g)=CO2(g)+2H2O(g);△H=-802.33kJ/mol,则CH4的燃烧热为802.33 kJ/mol |
| D、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则含20gNaOH的稀溶液与稀盐酸完全中和,中和热为28.65kJ/mol |
下列关于热化学反应的描述中正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、由C(s,石墨)═C(s,金刚石)△H=+1.9 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1,则CH3COOH和NaOH反应的生成1mo水时放出的热量为57.3 kJ |
| D、CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0 kJ/mol |
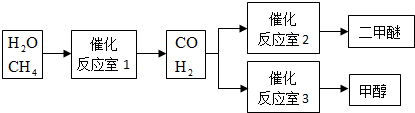
 研究工业废弃物的处理和防治具有重要的意义.
研究工业废弃物的处理和防治具有重要的意义.

