题目内容
利用下列实验装置能完成相应实验的是( )
A、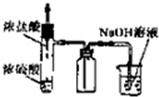 制取并吸收HCl |
B、 实验室制氨气 |
C、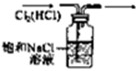 除去Cl2中的HCl |
D、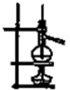 分离液体混合物 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.HCl能与氢氧化钠迅速反应;
B.遇冷后NH3和HCl马上化合为NH4Cl;
C.HCl易溶于水,而氯气难溶于饱和食盐水;
D.温度计时测量蒸汽的温度.
B.遇冷后NH3和HCl马上化合为NH4Cl;
C.HCl易溶于水,而氯气难溶于饱和食盐水;
D.温度计时测量蒸汽的温度.
解答:
解:A.HCl能与氢氧化钠迅速反应,应用倒置的漏斗防倒吸,故A错误;
B.NH4Cl受热分解为NH3和HCl,遇冷后NH3和HCl马上化合为NH4Cl,故B错误;
C.HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl,故C正确;
D.温度计时测量蒸汽的温度,应放在蒸馏烧瓶的支管口处,故D错误.
故选C.
B.NH4Cl受热分解为NH3和HCl,遇冷后NH3和HCl马上化合为NH4Cl,故B错误;
C.HCl易溶于水,而氯气难溶于饱和食盐水,所以可用饱和NaCl溶液除去Cl2中的少量HCl,故C正确;
D.温度计时测量蒸汽的温度,应放在蒸馏烧瓶的支管口处,故D错误.
故选C.
点评:本题考查较为综合,涉及物质制备以及分离提纯等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列溶液中,pH大于8的是( )
| A、在10 mL 0.2 mol/L的盐酸中加入9.99 mL 0.2 mol/L NaOH溶液后的溶液 |
| B、将pH=12的NaOH溶液稀释100倍后的溶液 |
| C、将pH=5的醋酸溶液稀释1000倍后的溶液 |
| D、c(OH-)=10-6mol/L的NaOH溶液10 mL加入10-5 mol/L的NaOH溶液100 mL后的溶液 |
| E、c(OH-)=10-6mol/L的NaOH溶液10 mL加入10-5 mol/L的NaOH溶液100 mL后的溶液 |
甲、乙两车间排放出的污水中分别含有大量且不同的4种离子,这些离子是Ag+、Ba2+、Fe3+、Na+、Cl-、NO3-、OH-、SO42-.经检测,甲车间的污水pH>7,则下列判断正确的是( )
| A、甲车间的污水中可能含有Ba2+ |
| B、乙车间的污水中可能含有Na+ |
| C、甲车间的污水中不可能含有SO42- |
| D、乙车间的污水中一定含有Fe3+ |
鉴别CH4、CO、H2三种无色气体的方法是( )
| A、点燃→通入澄清石灰水→加入溴的四氯化碳溶液 |
| B、点燃→罩上小烧杯→加入澄清石灰水 |
| C、点燃→通入澄清石灰水 |
| D、点燃→通入酸性KMnO4溶液 |
设某元素原子核内的质子数为12,质量数为24,则下述论断正确的是 ( )
| A、由此确定该元素的相对原子质量为24 |
| B、这种元素原子的近似相对原子质量为24 |
| C、若C-12原子质量为W g,此原子的质量约是为24W g |
| D、该原子核内中子的总质量近似等于质子的总质量 |
下列有关氧化物的说法正确的是( )
| A、凡是酸性氧化物,均可与水反应生成相应的酸 |
| B、非金属氧化物都是酸性氧化物 |
| C、碱性氧化物都是金属氧化物 |
| D、不能跟酸反应的氧化物,一定能跟碱反应 |
下列原子结构模型与科学家对应不正确的一项是( )
| A、阿伏加德罗的原子学说 |
| B、汤姆生的“葡萄干面包式”原子结构模型 |
| C、卢瑟福的带核原子结构模型 |
| D、玻尔的核外电子在一定轨道上运动的观点 |
下列分离或提纯混合物的方法正确的是( )
| A、除去NaCl固体中混有的MgCl2:加入KOH试剂后过滤 |
| B、用乙醇萃取碘水中的碘 |
| C、用溶解过滤蒸发的方法除去固体BaCl2中的BaSO4 |
| D、提纯含有少量硝酸钡杂质的硝酸钾溶液,加入过量硫酸钾溶液,过滤,滤液中补加适量硝酸 |
将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:Ag2SO4(s)?Ag2O(s)+SO3(g),2SO3(g)?2SO2(g)+O2(g),经10分钟后,反应达到平衡,此时C(SO3)=0.4mol/L,C(SO2)=0.1mol/L,则下列叙述不正确的是( )
| A、SO3的分解率为20% |
| B、平衡时,v(O2)=0.005 mol/(L?min) |
| C、容器内气体的密度为40g/L |
| D、加压,容器内固体质量不变 |