题目内容
3.(1)在甲烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 FeCl3 溶液,继续煮沸直至溶液呈红褐色,停止加热,即可以制得Fe(OH)3胶体.制备Fe(OH)3胶体的化学方程式:FeCl3+3H2O$\frac{\underline{\;△\;}}{\;}$3HCl+Fe(OH)3胶体(2)另取乙烧杯,加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,震荡均匀后,将乙烧杯与甲烧杯一起置于暗处,分别用激光笔照射烧杯中的液体,可以看到甲烧杯中的液体产生丁达尔效应.
(3)取甲烧杯中的少量Fe(OH)3胶体于试管中,向试管中逐滴滴加稀盐酸,
现象:先观察到沉淀,后沉淀溶解,原因:加入的盐酸是电解质,所以先使Fe(OH)3胶体聚沉,后发生酸碱中和反应,沉淀溶解.
分析 (1)饱和氯化铁在沸水中水解生成胶体;
(2)丁达尔现象为胶体特有的性质;
(3)Fe(OH)3胶体中逐滴滴加稀盐酸,先发生聚沉,后沉淀溶解.
解答 解:(1)甲烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3 溶液,继续煮沸直至溶液呈红褐色,停止加热,即可以制得Fe(OH)3胶体.制备Fe(OH)3胶体的化学方程式为FeCl3+3H2O$\frac{\underline{\;△\;}}{\;}$3HCl+Fe(OH)3胶体,
故答案为:饱和;红褐;FeCl3+3H2O$\frac{\underline{\;△\;}}{\;}$3HCl+Fe(OH)3胶体;
(2)甲为胶体分散系,乙为溶液,则分别用激光笔照射烧杯中的液体,可以看到甲烧杯中的液体产生一条光亮的通路,即丁达尔效应.
故答案为:甲;丁达尔效应;
(3)取甲烧杯中的少量Fe(OH)3胶体于试管中,向试管中逐滴滴加稀盐酸,现象为先观察到沉淀,后沉淀溶解,原因为加入的盐酸是电解质,所以先使Fe(OH)3胶体聚沉,后发生酸碱中和反应,沉淀溶解,反应的方程式为Fe(OH)3+3HCl=FeCl3+3H2O,
故答案为:先观察到沉淀,后沉淀溶解;加入的盐酸是电解质,所以先使Fe(OH)3胶体聚沉,后发生酸碱中和反应,沉淀溶解;
点评 本题考查了胶体和溶液、浊液性质的区别,应注意的是在氢氧化铁胶体中加入HCl电解质溶液后,先发生聚沉,后沉淀溶解.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
13.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到.现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液.电解开始不久,阴极区溶液呈红色,而阳极区溶液呈蓝色,同时有白色沉淀生成.下列说法中正确的是( )
| A. | 对阳极区溶液呈蓝色的正确解释是:2I--2e-=I2,碘遇淀粉变蓝 | |
| B. | 对阳极区溶液呈蓝色的正确解释是:Cu-2e-=Cu2+,Cu2+显蓝色 | |
| C. | 阴极区溶液呈红色的原因是:2H++2e-=H2↑,使阴极附近OH- 浓度增大,溶液显碱性,从而使酚酞变红 | |
| D. | 阴极上的电极反应式为:Cu2++2e-=Cu |
14.下列分子中的所有原子一定在同一平面上的是( )
| A. | 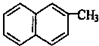 | B. | 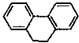 | C. | 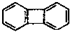 | D. | 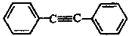 |
11.下列有机物在空气中燃烧的说法正确的是( )
| A. | 只有碳的氧化物和水 | |
| B. | 只有CO2和水 | |
| C. | 可能有碳的氧化物、水及其他元素的化合物 | |
| D. | 有CO、CO2、水及其他元素的化合物 |
15.25℃时,某一元弱酸HA的电离平衡常数为Ka,A?的水解平衡常数为Kh,该温度下向20mL 0.lmol•L-1 HA溶液中逐滴加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略反应导致的温度变化).下列说法不正确的是( )

| A. | 滴定过程中总是存在:Ka>Kh | |
| B. | 点②所示溶液中存在:c(Na+)=c(A-) | |
| C. | 点③所示溶液中存在:c(Na+)=c(A-)+c(HA) | |
| D. | 向点①所示溶液中加水:$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$比值减小 |
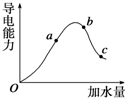 在25℃时,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
在25℃时,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: