题目内容
某化工厂排放的污水中含有Zn2+、Hg2+、Fe2+、Ag+等四种离子.某学生利用实验室可以提供的药品和仪器,综合考虑有关因素(如反应速率、经济效益、环境保护等),设计从该污水中回收金属银的
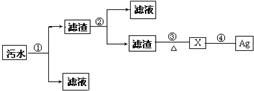
实验室可以提供的药品:锌粉、铜粉、铁粉、稀盐酸、稀硫酸、氢氧化钠溶液;可以提供的仪器:试管、烧杯、导管、铁架台(包括铁夹、铁圈、石棉网等)、酒精灯、U形管、启普发生器等.试填写下列空白:
(1)第①、②步操作中需要的药品为:① ;② .
(2)第③步操作的仪器必须连接 装置,理由是 .
(3)第④步操作必须的玻璃仪器为 ,实验过程中发生的主要现象是 .反应的化学方程式 .
(4)第④步操作开始时应该 ,结束时应该 .实验过程中对多余氢气的处理方法是 .

实验室可以提供的药品:锌粉、铜粉、铁粉、稀盐酸、稀硫酸、氢氧化钠溶液;可以提供的仪器:试管、烧杯、导管、铁架台(包括铁夹、铁圈、石棉网等)、酒精灯、U形管、启普发生器等.试填写下列空白:
(1)第①、②步操作中需要的药品为:①
(2)第③步操作的仪器必须连接
(3)第④步操作必须的玻璃仪器为
(4)第④步操作开始时应该
考点:物质的分离、提纯的基本方法选择与应用,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:银是不活泼的金属,可以用活泼的金属从溶液中置换出来,由于汞也不活泼,因此固体残渣中一定含有汞,虽然汞易挥发,但汞蒸汽有毒.所以在加热回收时必须加一个冷凝装置.因为加热时银将变成氧化银,所以需要用氢气还原.
(1)根据反应的原理和目的确定用到的试剂;
(2)汞易挥发,但汞蒸汽有毒;
(3)加热时银将变成氧化银,所以需要用氢气还原,可以得到金属银;
(4)氢气还原金属氧化物中的金属时,实验顺序是:先通氢气,后点灯,试管冷却再停止通入氢气.
(1)根据反应的原理和目的确定用到的试剂;
(2)汞易挥发,但汞蒸汽有毒;
(3)加热时银将变成氧化银,所以需要用氢气还原,可以得到金属银;
(4)氢气还原金属氧化物中的金属时,实验顺序是:先通氢气,后点灯,试管冷却再停止通入氢气.
解答:
解:银、汞是不活泼的金属,可以用活泼的金属铁将金属从溶液中置换出来,但是金属汞易挥发,汞蒸汽有毒,所以在加热回收金属银的时候必须加一个冷凝装置,将生成的金属汞冷却,此外因为加热时银将变成氧化银,所以需要用氢气还原来获得金属银.
(1)银、汞是不活泼的金属,可以用活泼的金属铁将金属从溶液中置换出来,即①操作的试剂是金属铁,然后过滤得到的滤渣含有金属银、汞以及剩余的金属铁,再加入稀盐酸或是稀硫酸过滤,即可以将金属银和金属汞滤出,即操作③的试剂是稀盐酸或稀硫酸,故答案为:铁粉;稀盐酸或稀硫酸;
(2)汞易挥发,但汞蒸汽有毒,第③步加热使汞和银分离实验仪器必须连接冷却回收,回收金属汞,防止汞蒸气污染环境,故答案为:冷却回收;回收金属汞,防止汞蒸气污染环境;
(3)加热时银将变成氧化银,所以需要用氢气还原,操作必须的玻璃仪器为试管、导管、酒精灯,发生反应:H2+Ag2O
2Ag+H2O,现象是:棕褐色固体变为银白色,试管口有水滴,故答案为:试管、导管、酒精灯;棕褐色固体变为银白色,试管口有水滴;H2+Ag2O
2Ag+H2O;
(4)氢气还原金属氧化物中的金属时,实验顺序是:先通氢气,后点灯,将装置中的空气排净,防止金属银和氧气发生反应,试管冷却再停止通入氢气,防止试管骤然冷却炸裂试管,氢气的尾气处理可以采用点燃法,故答案为:先通H2,待H2充满试管后,再加热;先停止加热,继续通H2,待试管冷却后停止通H2;点燃.
(1)银、汞是不活泼的金属,可以用活泼的金属铁将金属从溶液中置换出来,即①操作的试剂是金属铁,然后过滤得到的滤渣含有金属银、汞以及剩余的金属铁,再加入稀盐酸或是稀硫酸过滤,即可以将金属银和金属汞滤出,即操作③的试剂是稀盐酸或稀硫酸,故答案为:铁粉;稀盐酸或稀硫酸;
(2)汞易挥发,但汞蒸汽有毒,第③步加热使汞和银分离实验仪器必须连接冷却回收,回收金属汞,防止汞蒸气污染环境,故答案为:冷却回收;回收金属汞,防止汞蒸气污染环境;
(3)加热时银将变成氧化银,所以需要用氢气还原,操作必须的玻璃仪器为试管、导管、酒精灯,发生反应:H2+Ag2O
| ||
| ||
(4)氢气还原金属氧化物中的金属时,实验顺序是:先通氢气,后点灯,将装置中的空气排净,防止金属银和氧气发生反应,试管冷却再停止通入氢气,防止试管骤然冷却炸裂试管,氢气的尾气处理可以采用点燃法,故答案为:先通H2,待H2充满试管后,再加热;先停止加热,继续通H2,待试管冷却后停止通H2;点燃.
点评:本题主要考查混合物的分离除杂质知识,对于汞的易挥发而引起的环境污染,要充分注意,是一道化学和生活联系密切的题目,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
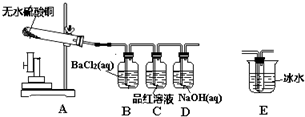
用下列实验装置进行相应实验,能达到实验目的,且实验装置正确的是( )


| A、图1所示装置,检验碳酸钾中钾元素的存在 |
| B、图2所示装置,称量少量氢氧化钠固体 |
| C、图3所示装置,分离CCl4萃取溴水后所得的有机层和水层 |
| D、图4所示装置,分离沸点相差较大的酒精、水的混合物 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中(放有等质量的纸) |

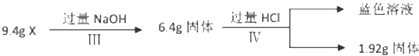
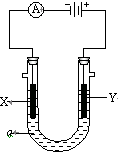 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: