题目内容
某化合物A是一种易溶于水的不含结晶水盐,溶于水后可完全电离出三种中学化学常见离子,其中有两种是10电子的阳离子.用A进行如下实验:取2.370gA溶于蒸馏水配成溶液;向该溶液中逐滴 加入一定量的氢氧化钠溶液,过程中先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体 C,气体不再产生时沉淀开始溶解,当沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol.回答下列问题:
(1)请画出沉淀B中金属元素的原子结构示意图 .
(2)化合物A的化学式为 ;请设计实验方案验证A中阴离子 ;
(3)请写出沉淀B溶解在氢氧化钠溶液中的离子方程式
(4)请写出气体C与氯气发生氧化还原反应的化学方程式 .
(1)请画出沉淀B中金属元素的原子结构示意图
(2)化合物A的化学式为
(3)请写出沉淀B溶解在氢氧化钠溶液中的离子方程式
(4)请写出气体C与氯气发生氧化还原反应的化学方程式
考点:无机物的推断,物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:由信息可知,A与NaOH溶液反应,先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体C,气体不再产生时沉淀开始溶解,则气体C为氨气,白色沉淀为氢氧化铝,A中含NH4+、Al3+,均为10电子的阳离子,沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol,由Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3.H2O、Al(OH)3+OH-=AlO2-+2H2O可知,NH4+、Al3+为1:1,则A中含阴离子带2个单位的负电荷,且与铵根离子、铝离子不反应,则阴离子可为SO42-,以此来解答.
解答:
解:由信息可知,A与NaOH溶液反应,先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体C,气体不再产生时沉淀开始溶解,则气体C为氨气,白色沉淀为氢氧化铝,A中含NH4+、Al3+,均为10电子的阳离子,沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol,由Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3.H2O、Al(OH)3+OH-=AlO2-+2H2O可知,NH4+、Al3+为1:1,则A中含阴离子带2个单位的负电荷,且与铵根离子、铝离子不反应,则阴离子可为SO42-,
(1)B中金属元素为A来,原子结构示意图为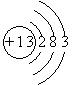 ,故答案为:
,故答案为: ;
;
(2)由上述分析可知A为NH4Al(SO4)2,检验A中阴离子的方法为取少量A的溶液于试管中,加入足量的稀盐酸酸化,再加入氯化钡,若有白色沉淀生成,说明A中的阴离子为硫酸根离子,故答案为:NH4Al(SO4)2;取少量A的溶液于试管中,加入足量的稀盐酸酸化,再加入氯化钡,若有白色沉淀生成,说明A中的阴离子为硫酸根离子;
(3)B溶解在氢氧化钠溶液中的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)C与氯气发生氧化还原反应的化学方程式为3Cl2+8NH3=N2+6NH4Cl,故答案为:3Cl2+8NH3=N2+6NH4Cl.
(1)B中金属元素为A来,原子结构示意图为
 ,故答案为:
,故答案为: ;
;(2)由上述分析可知A为NH4Al(SO4)2,检验A中阴离子的方法为取少量A的溶液于试管中,加入足量的稀盐酸酸化,再加入氯化钡,若有白色沉淀生成,说明A中的阴离子为硫酸根离子,故答案为:NH4Al(SO4)2;取少量A的溶液于试管中,加入足量的稀盐酸酸化,再加入氯化钡,若有白色沉淀生成,说明A中的阴离子为硫酸根离子;
(3)B溶解在氢氧化钠溶液中的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)C与氯气发生氧化还原反应的化学方程式为3Cl2+8NH3=N2+6NH4Cl,故答案为:3Cl2+8NH3=N2+6NH4Cl.
点评:本题考查无机物的推断,为高频考点,把握铵根离子、铝离子的检验为解答的关键,注意阴离子可由电荷守恒分析,侧重分析与推断能力的综合考查,题目难度中等.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
将某无色气体X通入品红溶液,溶液褪色;加热,溶液又变红色.X可能是( )
| A、O2 |
| B、SO2 |
| C、Cl2 |
| D、CO2 |
已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、
CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等.为了进一步探究该水溶液的组成,某同 学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
③另取溶液加入BaCU溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等.为了进一步探究该水溶液的组成,某同 学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
③另取溶液加入BaCU溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
| A、无法确定溶液中是否存在Cu2+离子 |
| B、原溶液中不含K+、Al3+、CO3I等离子 |
| C、根据步骤②只能确定溶液中一定存在NO3-离子 |
| D、步骤③所得到的白色沉淀共有2种钡盐 |







 A、B、C、D、E、X六种元素的原子序数依次递增,A、B、C的基态原子中L层未成对电子数分别为3、2、1,D是短周期中原子半径最大的主族元素,E是主族元素且与X同周期,E与C可形成离子化合物,其晶胞结构如图所示.X位于元素周期表中第四周期ⅠB族.
A、B、C、D、E、X六种元素的原子序数依次递增,A、B、C的基态原子中L层未成对电子数分别为3、2、1,D是短周期中原子半径最大的主族元素,E是主族元素且与X同周期,E与C可形成离子化合物,其晶胞结构如图所示.X位于元素周期表中第四周期ⅠB族.