题目内容
14.“套管实验”是将一支较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要更多仪器进行的实验,因其具有许多优点,被广泛应用于化学实验中,如图1实验为“套管实验”,小试管内塞有沾有无水硫酸铜粉末的棉花糖.请观察实验装置,分析实验原理.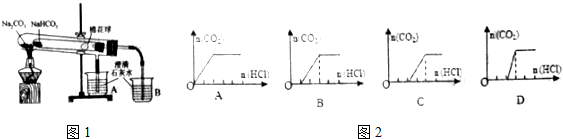
回答下列问题:
(1)该实验的目的是探究(或证明)碳酸氢钠不稳定,受热易分成解产生CO2和H2O,而碳酸钠稳定.
(2)该实验的现象是棉花糖上的粉末变蓝、B中澄清石灰水变浑浊,B中发生反应的离子方程式是Ca2++2OH-+CO2=CaCO3↓+H2O.
(3)一段时间后结束实验,待装置冷却,取出小试管中固体溶于水,然后滴加1mol/L盐酸,产生CO2的量与盐酸的量的关系如图2所示,其中合理的是B、C.
(4)取10.0g碳酸钠和碳酸氢钠的混合物充分进行加热,将生成的CO2气体通入足量澄清石灰水中完全吸收,测得生成沉淀4.0g,则原混合物中碳酸钠的质量分数为32.8%.
分析 (1)碳酸氢钠受热易分解,小试管中为碳酸氢钠,说明温度低时可分解;
(2)碳酸氢钠分解生成二氧化碳,二氧化碳使石灰水变浑浊;
(3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,则加热一段时间后固体为Na2CO3或Na2CO3、NaHCO3,结合NaHCO3+HCl=NaCl+CO2↑+H2O、Na2CO3+2HCl=2NaCl+CO2↑+H2O及图象解答;
(4)发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Ca2++2OH-+CO2=CaCO3↓+H2O,可知2NaHCO3~CaCO3,以此计算.
解答 解:(1)碳酸氢钠受热易分解,小试管中为碳酸氢钠,说明温度低时可分解,而碳酸钠受热温度高,碳酸钠不分解,所以该实验的目的是探究(或证明)碳酸氢钠不稳定,受热易分成解产生CO2和H2O,而碳酸钠稳定,
故答案为:探究(或证明)碳酸氢钠不稳定,受热易分成解产生CO2和H2O,而碳酸钠稳定;
(2)碳酸氢钠分解生成二氧化碳,棉花糖上的粉末变蓝,B中澄清石灰水变浑浊,B中离子反应为Ca2++2OH-+CO2=CaCO3↓+H2O,
故答案为:棉花糖上的粉末变蓝、B中澄清石灰水变浑浊;Ca2++2OH-+CO2=CaCO3↓+H2O;
(3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,则加热一段时间后固体为Na2CO3或Na2CO3、NaHCO3,
若完全分解,只有碳酸钠,由Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl=NaCl+CO2↑+H2O可知,开始不生成气体,且生成气体和不生成气体时消耗酸相同,图象C符合;
若部分分解,则固体为Na2CO3、NaHCO3,由NaHCO3+HCl=NaCl+CO2↑+H2O、Na2CO3+2HCl=2NaCl+CO2↑+H2O可知,开始不生成气体,但生成气体消耗的酸大于不生成气体时消耗的酸,图象B符合,
故答案为:B、C;
(4)发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Ca2++2OH-+CO2=CaCO3↓+H2O,可知2NaHCO3~CaCO3,n(CaCO3)=$\frac{4.0g}{100g/mol}$=0.04mol,则n(NaHCO3)=0.08mol,则原混合物中碳酸钠的质量分数为$\frac{10.0g-84g/mol×0.08mol}{10.0g}$×100%=32.8%,故答案为:32.8%.
点评 本题考查性质实验方案的设计,为高频考点,把握碳酸氢钠的不稳定性及实验装置的作用为解答的关键,注意(3)中固体成分、发生的反应及图象关系为解答的难点,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| 实验编号 | 溶液体积(mL) | 反应后溶液的pH | |
| HA | KOH | ||
| ① | 10 | 10 | |
| ② | 10 | a | 7 |
| A. | 实验①所得的混合溶液中:c(K+)>c(A-)>c(H+)>c(OH-) | |
| B. | 实验①所得的混合溶液中:c(OH-)+c(A-)=c(K+)+c(H+) | |
| C. | 实验②所得的混合溶液中:c(A-)+c(HA)=0.1mol•L-1 | |
| D. | 实验②所得的混合溶液中:(K+)>c(A-)>c(OH-)=c(H+) |
| A. | 萃取操作时,应选择有机萃取剂,萃取剂的密度不一定比水大 | |
| B. | 检验溶液中是否有SO42-时,加入BaCl2溶液,再加稀硝酸,观察沉淀是否消失 | |
| C. | 以酚酞为指示剂向盐酸中滴加氢氧化钠溶液时,滴定终点时溶液由粉红色恰好变为无色 | |
| D. | 酸式滴定管、碱式滴定管、移液管都是准确量取一定体积液体的容器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 |

下列说法正确的是( )
| A. | NaOH溶液可以用氨水来代替 | |
| B. | 溶液a中含有Al3+、K+、Cl-、Na+、OH- | |
| C. | 溶液b中只含有NaCl | |
| D. | 向溶液a中滴加盐酸需控制溶液的pH |
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 澄清的石灰水与稀盐酸反应 Ca (OH)2+2H+═Ca2++2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| A. | 在无色溶液中:Na+、Fe2+、Cl-、SO42- | |
| B. | 在酸性溶液中:NH4+、Ca2+、NO3-、HCO3- | |
| C. | 在碱性溶液中:K+、Ba2+、SO42-、NO3- | |
| D. | 在含大量Mg2+的溶液中:Na+、NH4+、SO42-、Cl- |
| A. | 干冰、铝粉、漂白粉 | B. | 生石灰、臭氧、熟石灰 | ||
| C. | 烧碱、液态氧、酒精 | D. | 铁红、晶体硅、胆矾 |
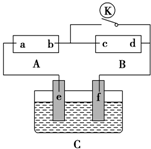 如图所示,A为直流电源,B为浸透饱和硫酸钠溶液和紫色石蕊溶液的滤纸,C为电镀池,接通电路后,发现B上的c点显蓝色,请填空:
如图所示,A为直流电源,B为浸透饱和硫酸钠溶液和紫色石蕊溶液的滤纸,C为电镀池,接通电路后,发现B上的c点显蓝色,请填空: