题目内容
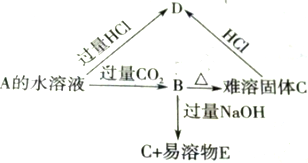 A、B、C、D、E 5种物质的转化关系如图所示.已知A为二元碱,微溶于水且溶解度随温度升高而降低
A、B、C、D、E 5种物质的转化关系如图所示.已知A为二元碱,微溶于水且溶解度随温度升高而降低(1)写出各物质的化学式:A:
(2)写出下列两个变化的离子方程式:B→D:
(3)E溶液中混有一定量的NaOH,可通过哪种途径得到纯净的固体E?
考点:无机物的推断
专题:
分析:A为二元碱,微溶于水且溶解度随温度升高而降低,则A可能为Ca(OH)2,由转化关系可知,D为CaCl2,B为Ca(HCO3)2,C为CaCO3,E为Na2CO3,验证符合转化关系,据此解答.
解答:
解:(1)A为二元碱,微溶于水且溶解度随温度升高而降低,则A可能为Ca(OH)2,由转化关系可知,D为CaCl2,B为Ca(HCO3)2,C为CaCO3,E为Na2CO3,验证符合转化关系,
故答案为:Ca(OH)2;Ca(HCO3)2;CaCO3;CaCl2;Na2CO3;
(2)B→D的转化为碳酸氢钙与盐酸反应生成氯化钙、二氧化碳与水,反应离子方程式为:HCO3-+H+=CO2↑+H2O;
B→E的转化是碳酸氢钙与过量氢氧化钠反应生成碳酸钙、碳酸钠与水,反应离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,
故答案为:HCO3-+H+=CO2↑+H2O;Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O;
(3)碳酸钠溶液中混有一定量的NaOH,可向该溶液中通入足量CO2使Na2CO3与NaOH转化为NaHCO3然后蒸干溶液并灼得到Na2CO3固体,
答:向碳酸钠溶液中通入足量CO2使Na2CO3与NaOH转化为NaHCO3然后蒸干溶液并灼得到Na2CO3固体.
故答案为:Ca(OH)2;Ca(HCO3)2;CaCO3;CaCl2;Na2CO3;
(2)B→D的转化为碳酸氢钙与盐酸反应生成氯化钙、二氧化碳与水,反应离子方程式为:HCO3-+H+=CO2↑+H2O;
B→E的转化是碳酸氢钙与过量氢氧化钠反应生成碳酸钙、碳酸钠与水,反应离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,
故答案为:HCO3-+H+=CO2↑+H2O;Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O;
(3)碳酸钠溶液中混有一定量的NaOH,可向该溶液中通入足量CO2使Na2CO3与NaOH转化为NaHCO3然后蒸干溶液并灼得到Na2CO3固体,
答:向碳酸钠溶液中通入足量CO2使Na2CO3与NaOH转化为NaHCO3然后蒸干溶液并灼得到Na2CO3固体.
点评:本题考查无机物推断、物质的分离提纯,难度中等,需要学生熟练掌握元素化合物的知识,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各离子组可在同一溶液中大量共存,且形成无色溶液的是( )
| A、Fe2+、H+、NO3-、Cl- |
| B、Cu2+、Ba2+、Cl-、NO3- |
| C、Na+、Mg2+、OH-、SO42- |
| D、K+、Na+、OH-、NO3- |
下列含有相同元素的化合物组是( )
| A、O2、O3 |
| B、CO、CO2 |
| C、KCl、AlCl3 |
| D、NaHCO3、NaHSO4 |
如图所示的钢铁腐蚀中下列说法正确的是( )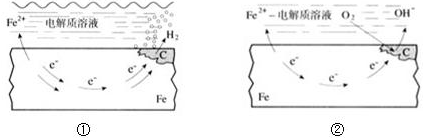

| A、碳表面发生氧化反应 |
| B、钢铁被腐蚀的最终产物为FeO |
| C、生活中钢铁制品的腐蚀以图①所示为主 |
| D、图②中,正极反应式为O2+4e-+2H2O═4OH- |
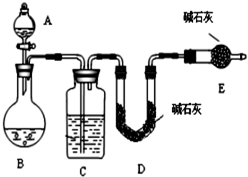 某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数